【物质结构与性质】晶体的熔、沸点大小比较|重要题型 方法梳理

【晶体熔沸点大小】
一、解题步骤
1)判断常温常压下物质聚集状态:
- 固体>液体>气体
2)分析物质所属晶体类型:
- 共价晶体>离子晶体>分子晶体
- 离子晶体熔点高,熔融态可导电
3)抓住决定同类晶体熔、沸点高低主要因素
①共价晶体:共价晶体熔化时需要破坏共价键,因此在结构相似的共价晶体中,原子半径越小,共价键键长越短,键能越大,熔点就越高

②离子晶体:由于晶体熔化时需要破坏离子键,对于AB型(Nacl)的离子晶体,阴阳离子所带电荷数越多(主要因素)、离子半径越小(次要因素),离子间的作用力越强,熔点就越高。

- 晶格能:气态阳离子&气态阴离子形成1mol固态晶体所释放的能量
③金属晶体:金属原子半径越小,价电子数越多,金属键越强,金属晶体的熔点越高

- 看清是金属键能还是金属性

④分子晶体:分子晶体熔化或汽化时,破坏的是分子间作用力(氢键、范德华力),因此分子晶体的熔沸点大小需要判断的是分子间作用力的大小
- i.比较分子晶体熔沸点优先考虑氢键,在相对分子质量相近的分子中,多氢键分子>单氢键分子>无氢键分子

一分子H2O含有两个氢键
- ii.分子间氢键与分子内氢键对熔沸点的影响:分子内形成氢键,相应的分子间作用力就会减小,该物质的熔沸点比同系列物质的熔沸点低

- iii.若无氢键且组成和结构相似的分子晶体,相对分子质量越大,范德华力越大,熔沸点越高

- iv.若无氢键且相对分子质量相近,分子的极性越大,范德华力越大,熔沸点越高
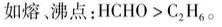
- iiv.对于有机化合物的同分异构体而言,支链越多,沸点越低

二、例题








