一化 | P21【钠及化合物】【一化辞典】2 单质钠和钠的氧化物



1️⃣钠单质的物理性质
1. 颜色:银白色,有金属光泽
2. 密度:ρ(H₂O) >ρ(Na)>ρ(煤油)
3. 熔点:低于100°C
4. 硬度:质地柔软,轻压变形,可以用小刀切割
2️⃣钠的化学性质
从钠原子的原子结构认识钠的化学性质——还原性

钠单质与氧气的反应
4Na + O₂ = 2Na₂O
2Na + O₂ = Na₂O₂
Na—O₂→Na₂O—H₂O→NaOH—CO₂→Na₂CO₃·10H₂O—→Na₂CO₃
钠单质与水的反应
化学方程式:2Na + 2H₂O = 2NaOH + H₂
离子方程式:2Na + 2H₂O = 2Na⁺ + 2OH⁻ + H₂
现象:浮熔游响红
浮:钠浮在水面上(ρ(H₂O) >ρ(Na))
熔:①Na熔点低;②Na的反应很剧烈,放出很大热量
游&响:反应释放出气体,气体推动Na移动;发生响声
红:最终生成NaOH碱性物质
钠单质与盐溶液的反应
2Na + 2H₂O = 2NaOH + H₂
CuSO₄ + 2NaOH = Na₂SO₄ + Cu(OH)₂
Na放入到饱和NaOH溶液,会让NaOH析出
钠单质知识点,你学会了吗?
(1)钠是银白色金属,熔点低,硬度大(x)【硬度小】
(2)金属钠在自然界中只能以化合物的形式存在(✓)
(3)钠在反应时,只能作还原剂(✓)【金属单质只能做还原剂】
(4)在空气中加热时,金属钠剧烈燃烧,产生黄色火焰和白色固体(x)【Na₂O₂是淡黄色固体】
(5)钠与O₂反应只能生成淡黄色固体Na₂O₂(x)【还能生成Na₂O】
(6)钠与H₂O反应比钠与盐酸反应更剧烈(x)【盐酸更剧烈】
(7)将金属钠投入硫酸铜溶液中,钠迅速反应,产生红色固体(x)【蓝色固体和气体】
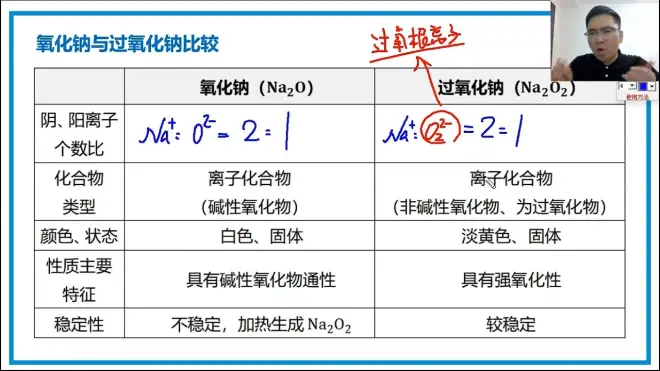
氧化纳与过氧化钠比较