高中化学基础与解法全集(涵盖所有)|长期更新|从零开始拯救所有学渣!

元素周期律



化学键

【有机化合物】【一化辞典】3同分... P79 - 02:23
热力学
【选必一 化反热效应】【一化词典... P87 - 00:00
溶液中的电荷守恒




【选必一 溶液离子平衡】【一化... P113 - 16:31
沉淀溶解平衡图像P121
原电池P123
1.概念
本质:自发的氧化还原反应
记忆正负极:负失氧,正得还

2.(单/双液原电池)

3.原电池正负极判断(重要)
升失氧化还原剂,降得还原氧化剂


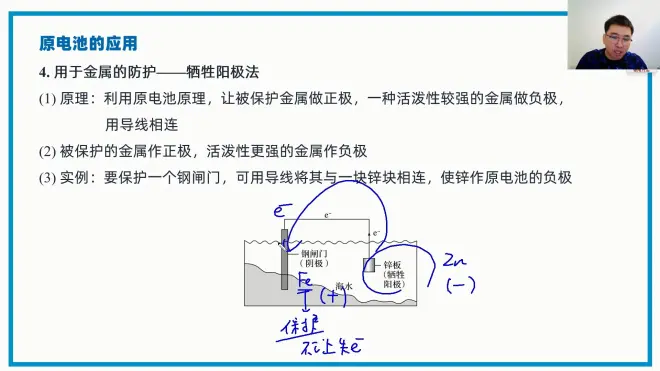
4.原电池的应用
加快反应速率;比较金属活动性
一般负极活动性强,
反例:Mg和Al(Mg2+会和NaOH反应生成Mg(OH)2,但Mg不会)
Fe和Cu在浓H2SO4中(铁会钝化)

(石磨棒只导电不反应)

保护:不让他失电子