辉瑞、盐野义3CL蛋白酶抑制剂,默沙东RdRp抑制剂即将会师国内
——快 讯——
12月30日,国家药监局按照药品特别审批程序附条件批准默沙东新冠病毒治疗药物莫诺拉韦胶囊(商品名称:利卓瑞/LAGEVRIO,Molnupiravir),用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒感染(COVID-19)患者,例如伴有高龄、肥胖或超重、慢性肾脏疾病、糖尿病、严重心血管疾病、慢性阻塞性肺疾病、活动性癌症等重症高风险因素的患者。
这条消息没有什么疑惑点,毕竟也是已经获得FDA批准的新冠治疗药物,国内获批实属正常,让我疑惑的是下面的消息。
12月29日,中国生物制药发布公告称,公司附属公司正大天晴与平安盐野义签订独家市场推广协议。据此,正大天晴获授予Ensitrelvir在中国大陆地区的独家市场推广权,初步为期五年。
这里就牵扯到我一条之前追踪的消息:全球第二款获批的3CL蛋白酶抑制剂为日本盐野义制药研发的Ensitrelvir(Xocova),日前,盐野义发布消息称,为了在中国稳定供应已在日本获得紧急批准的新冠治疗药,该公司已与当地企业展开合作。合作方为中国大型制药企业“上海医药”旗下专门从事流通销售业务的子公司。如果新冠治疗药在中国获批,将从日本出口,并由该子公司独家负责中国市场的批发销售。
按我的理解,是上海医药旗下的流通子公司负责配送Xocova,正大天晴负责Xocova在相关诊疗机构的销售?有相关了解的人士可以后台留言。
另一款全球首个获批的3CL蛋白酶抑制剂Paxlovid也频传消息,Paxlovid于今年2月在国内获批上市,此前曾以2300元/盒的价格被临时纳入医保,在医保定点医院处方Paxlovid即可享受医保报销待遇。同时,近期还有网传消息称,北京计划在各社区医院配置Paxlovid,对社区医生进行培训后,由社区医生指导辖区内新冠患者服用进行抗病毒治疗,相关费用纳入北京医保甲类报销。在近期即将举行的医保谈判中,也有传言,Paxlovid将进行降价。
综上所述,由于传播率实在是广泛,且有恐慌情绪发酵,对于最新治疗药物的快速批准势在必行。那接下来,还是在既往对Paxlovid、Molnupiravir的非头对头比较中,增加Ensitrelvir的试验整理,同时,对重症住院患者使用的托珠单抗的信息进行再次整理,以飨读者。
——SARS-CoV-2——
SARS-CoV-2
SARS-CoV-2(新型冠状病毒)是一种有包膜的正义单链RNA病毒,基因组大小约为 29.9 kb。可以编码4个结构蛋白 (S, E, M和N) 和16个非结构蛋白 (nsp1-16)。最外层是刺突糖蛋白 (S, Spike Protein), 刺突下面是病毒包膜:由膜糖蛋白 (M, Membrane Protein) 和小包膜糖蛋白 (E, Envelope Protein) 构成, 包膜的内部是一个RNA基因链条和核衣壳蛋白 (N, Nucleocapsid Protein) 构成的螺旋折叠结构。

SARS-CoV-2的结构
SARS-CoV-2 Spike Protein
SARS-CoV-2的Spike Protein由两个功能亚基组成:S1亚基和S2亚基。S1亚基由N端结构域 (NTD) 和受体结合结构域 (RBD) 组成。S1亚基的功能是与宿主细胞上的受体结合。S2亚基包含FP, HR1, CH, CD, HR2, TM和CT。S2亚基的功能是融合病毒和宿主细胞的细胞膜。S1和S2亚基边界处的裂解位点称为S1/S2蛋白酶裂解位点。对于所有冠状病毒,宿主蛋白酶在S2切割位点切割刺突糖蛋白,激活蛋白质,改变刺突蛋白构象,通过不可逆构象变化融合病毒和宿主细胞的膜。

Spike 蛋白与细胞结合示意图
简而言之,SARS-CoV-2是一种RNA病毒,主要通过Spike蛋白(S蛋白,突刺糖蛋白)结合宿主细胞上的细胞表面受体ACE2(血管紧张素转换酶2)。S蛋白S1亚单位的N端结构域(S1-NTD)和C端结构域(S1-CTD)都能作为受体结合域(RBD)。一般认为S1-NTD结合糖类受体,S1-CTD结合蛋白类受体。继而病毒基因组通过以下两种方式进入宿主细胞质:
在被丝氨酸蛋白酶TMPRSS2切割和激活后直接与质膜融合;
利用宿主细胞的内吞机制,内吞病毒粒子在内核体中经历一系列激活步骤。
病毒基因组也作为信使RNA发挥作用,通过宿主细胞机制翻译出一系列蛋白质,如3CLPro(3C样蛋白酶)、PLpro(木瓜蛋白酶样半胱氨酸蛋白酶)和RdRp(RNA依赖性RNA聚合酶)。
SARS-CoV-2基因组还编码结构蛋白(S)、包膜蛋白(E)、膜蛋白(M)和核衣壳蛋白(N)。RdRP对病毒复制至关重要,因此是抗SARS-CoV-2药物的一个有吸引力的靶点。
简而言之,抗新冠病毒感染的药物作用机制可以归纳为两大类:
SARS-CoV-2的感染机制及潜在治疗靶点
一类是阻止病毒和宿主细胞结合,如S蛋白和ACE2,也是单克隆抗体药物经常采用的靶点;
SARS-CoV-2的感染机制及潜在治疗靶点
另一类是阻止新病毒在宿主细胞内的产生,可作用的靶点如3CLPro,PLpro、RdRp等。这些靶点也是潜在抗新冠病毒感染的小分子药物常采用的靶点。如Paxlovid是3CLPro抑制剂;Molnupiravir是一种核苷类似物,作用靶点为RdRp。
对于疫苗的相关研究,可能现阶段,更为关注的是口服特效药的进展,遂接下来,主要聚焦新冠口服药的作用机制和代表药物。
新冠口服药物的作用机制
Molnupiravir 疗效
Molnupiravir是一种核苷类似物,作用靶点为RdRp。
Molnupiravir 的III期MOVe-OUT研究中期数据表明,Molnupiravir降低了约50%的住院率或死亡风险,7.3%接受Molnupiravir的患者在随机分组后的第29天住院或死亡,而安慰剂治疗的患者有14.1%。在第29天时,在接受Molnupiravir的患者中没有死亡报告,而在接受安慰剂的患者中,有8人死亡。在Molnupiravir和安慰剂组中,发生的任何级别不良事件分别为35%和40%。药物相关不良事件的发生率分别为12%和11%,与安慰剂组(3.4%)相比,Molnupiravir组(1.3%)因不良事件而停止治疗的受试者较少。
Paxlovid作用机制
早在2002年,为了应对SARS病毒(SARS-CoV-1),辉瑞公司就开始尝试研发3CL蛋白酶抑制剂,并发现其研究的产品PF-00835231,在体外实验中,它能够强力抑制SARS-CoV-1的3CL蛋白酶活性。3C样蛋白酶(3CLpro)又称主要蛋白酶(Mpro),由306个氨基酸组成,可进一步切割新冠多聚蛋白,从而产生解旋酶、RNA依赖的RNA聚合酶等相关复制元件,在病毒增殖和组装中具有重要作用。天然的3CLpro单体由三个结构域组成,两个单体相互作用形成包含底物结合位点的口袋结构。活性中心位于结构域I和II之间的缝隙中,催化位点为145位的Cys和41位的His。
SARS-CoV-2 Mpro的三维结构
SARS病毒和新冠病毒的3CL蛋白酶在与底物结合的位点上具有100%的序列同源性,这意味着它也很可能对新冠病毒的3CL蛋白酶具有强力的抑制效果。辉瑞在PF-00835231的基础上进行了结构修饰,并做成口服药物,由此推动Paxlovid进入临床。
Paxlovid疗效
2021年11月5日,辉瑞(Pfizer)公司宣布,在研口服抗病毒疗法在2/3期临床试验中显著降低新冠患者住院率和死亡风险。基于积极的临床结果,独立数据监查委员会建议提前结束临床试验。
这项2/3期临床试验在非住院新冠患者中进行,患者在新冠症状出现3天内接受治疗。试验结果显示,与安慰剂组相比,Paxlovid将患者住院或死亡的风险降低了89%。在Paxlovid组,0.8%(3/389)的患者在28天内需要住院,对照组中这一比例为7.0%(27/385)。而且,在对照组中有7名患者不幸去世,Paxlovid组这一数值则为0。
Molnupiravir与Paxlovid的比较
首先说明一点,由于是不同的试验,直接拿来对比是不严谨的。但仅从各自的试验结果来分析其有效性,似乎Paxlovid更具有优势,Paxlovid能够将住院/死亡风险降低89%,Molnupiravir只能够降低50%。另外,从原理上来说,Paxlovid直接抑制了新冠病毒RNA聚合酶的作用,阻断了病毒复制过程;而Molnupiravir并没有阻断RNA的复制,而是通过给病毒“假”的核苷类似物,来替代C和G碱基,从而生成突变的遗传物质。但突变之后的RNA所组成的变异病毒是否还有毒性,这仍然有待进一步的研究验证。
Ensitrelvir
Ensitrelvir与辉瑞Paxlovid同属于新型3CL蛋白酶抑制剂,通过选择性地抑制3CL蛋白酶从而抑制SARS-CoV-2的增殖。
在盐野义公布的Ensitrelvir IIb期研究结果中,研究者评估了各组中病毒滴度阳性的患者比例。相比安慰剂组,第4天低剂量组和高剂量组病毒滴度阳性患者比例分别下降了98.1%和94.6%,均达到显著性差异。病毒滴度阳性转阴所需时间方面,低剂量组和高剂量组较安慰剂组分别缩短了40小时和30小时,显示出迅速清除病毒的作用。
后续进行的III期临床试验结果显示,在入组的1821名轻症至中等症状患者中(无论其是否有重症化风险或是否接种过疫苗),Ensitrelvir针对奥密克戎毒株典型的COVID-19五大症状(鼻塞╱流涕、喉咙酸痛、咳嗽、发热和疲倦)均有明显改善,症状消失时间达到了主要终点,同时在次要终点病毒滴度转阴时间上也显著优于安慰剂。
在安全性方面,根据II期及III期临床试验结果,未发现有严重不良事件及副作用。同时由于Ensitrelvir不需使用其他药物作为增强剂,减少药物相互作用的风险,对可能合并其他基础疾病的老年患者的依从性较佳。
——快 讯——
2022年12月21日,罗氏宣布,FDA已批准雅美罗®(托珠单抗)静脉注射(IV)用于治疗新型冠状病毒肺炎的成人住院患者,这些患者正在接受全身性皮质类固醇并需要补充氧气、无创或有创机械通气或体外膜氧合(ECMO)。托珠单抗是FDA批准的第一个治疗新冠肺炎的单克隆抗体,并被建议单次60分钟静脉输注。
2022年12月9日,百奥泰(688177.SH)公告,公司向FDA递交了BAT1806(托珠单抗)注射液的生物制品上市申请,并于近期收到了美国FDA受理的通知。据悉,BAT1806是百奥泰根据国家药品监督管理局、美国FDA、欧洲EMA生物类似药相关指导原则开发的托珠单抗注射液。
两条消息,让我突然发觉,既往做的有关新冠相关药物研究进展的梳理还有知识盲区,对于单克隆抗体在新冠领域的研究知之甚少。而托珠单抗作为早已有之的单克隆抗体,也有必要对其机理进行汇总,且自己正好也处于疑似患阳状态,周边的得病率高的离谱。只有足够了解,才能做到不惑,那就开始今晚的整理吧。
——托珠单抗注射液——
托珠单抗注射液,是一款靶向白介素-6受体(IL-6R)的重组人源化单克隆抗体,可与可溶性和膜结合型IL-6受体(sIL-6R和mIL-6R)特异性结合,并抑制由sIL-6R或mIL-6R介导的信号传导。既往的研究表明,IL-6是一种促炎性细胞因子,它的释放可以诱发一系列下游的促炎症反应。研究发现,IL-6也是诱发COVID-19患者体内细胞因子风暴的重要通路,而托珠单抗有可能减轻COVID-19患者的细胞因子风暴。
具体而言,部分新冠肺炎患者出现严重并发症,包括急性呼吸窘迫综合征(ARDS),甚至进入重症监护病房(ICU)并死亡。尸检活检样本分析表明,异常宿主免疫反应和炎性细胞因子风暴是导致新冠肺炎患者高死亡率的原因。
既往研究表明,致病性T细胞和炎性单核细胞通过大量白介素6(IL-6)引发炎症风暴.因此,靶向IL-6途径的单克隆抗体可能会抑制炎症风暴。

新冠肺炎患者“炎症风暴”产生机制

Tocilizumab通过阻断IL-6受体来平息炎症风暴
共有4项随机对照研究评估了托珠单抗在住院患者中治疗 COVID-19 的疗效,包括牛津大学领导的RECOVERY试验,以及罗氏赞助的EMPACTA、COVACTA和REMDACTA试验。FDA的批准是基于RECOVERY试验以及EMPACTA试验的结果。
RECOVERY 研究
研究背景
本研究旨在评估托珠单抗对因缺氧和全身炎症住院的新冠肺炎成人患者的治疗效果。
研究方法
RECOVERY研究为一项随机、对照、开放标签研究,旨在评估英国新冠肺炎住院患者的几种可能的治疗方法;
那些有缺氧(空气中氧饱和度<92%或需要氧治疗)和全身炎症证据(C反应蛋白≥75 mg/L)的试验参与者有资格按照1:1的比例进行随机分配,与常规护理标准和静脉注射400 mg–800 mg(取决于体重)的托珠单抗进行比较,如果患者的病情没有改善,可在12–24小时后再注射第二剂托珠单抗;
Tocilizumab的具体用量
IV over 60min + usual standard care
>90kg = 800mg
>65kg & ≤90kg = 600mg
>40kg & ≤65kg = 400mg
≤40kg = 8mg/kg
2nd dose could be given 12 to 24hrs later if patient’s condition had not improved
主要研究结果是在意向治疗人群中进行评估的28天死亡率;
该试验在ISRCTN(50189673)和ClinicalTrials.gov(NCT04381936)注册。
研究结果

Trial profile
2020年4月23日至2021年1月24日,共有21550名接受RECOVERY试验的患者,其中4116名成年人参与了托珠单抗的评估,其中3385名(82%)患者接受了系统性皮质类固醇治疗;
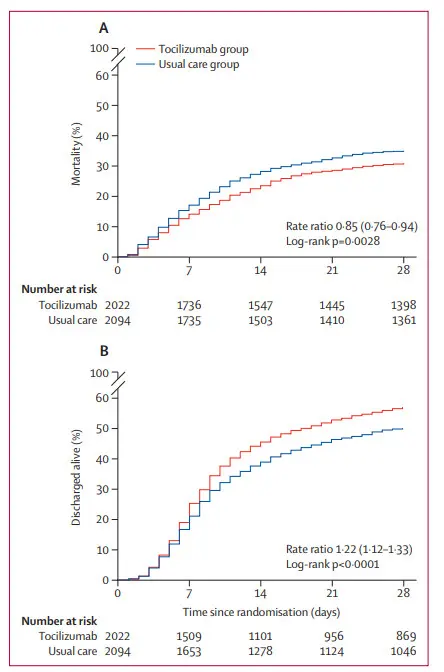
Effect of allocation to tocilizumab on 28-day mortality (A) and discharge from hospital within 28 days of randomisation (B)
总体而言,2022名接受托珠单抗治疗的患者中有621名(31%)在28天内死亡,2094名接受常规护理的患者中,有729名(35%)在28天后死亡(比率 0.85;95% Cl 0.76–0.94;p=0.028);
在所有预先指定的亚组患者中,包括接受全身皮质类固醇治疗的患者,均观察到一致的结果。分配给托珠单抗的患者更有可能在28天内出院(57% vs 50%;比率为1.22;1.12–1.33;p<0.0001);
在基线时未接受有创机械通气的患者中,分配托珠单抗的患者达到有创机械通风或死亡的复合终点的可能性较小(35%对42%;风险比0.84;95%CI 0.77–0.92;p<0.0001)。
研究结论
在患有缺氧和全身炎症的住院新冠肺炎患者中,托珠单抗改善了生存率结果。
结语
新冠口服药有望与新冠疫苗、中和抗体和其它新冠疗法一起,为人们提供多重保护,遏制疫情的发展蔓延。口服小分子药物为未接种疫苗,或对疫苗反应不佳的免疫功能低下人群,提供了一种防止疾病加重的方法。期望随着疫苗接种率的提升和相关治疗药物的问世,疫情对于世界生产和生活的冲击能够早日消弥。

