Neuron: 改善AD的新思路—降低胶质细胞脂质积聚和胆固醇代谢水平
2023年11月16日,圣路易斯华盛顿大学医学院(Washington University School of Medicine,WUSM)的研究者Neuron上发表了篇名为“Amelioration of Tau and ApoE4-linked glial lipid accumulation and neurodegeneration with an LXR agonist” 的研究型论文,其中第一作者为 Alexandra Litvinchuk 博士。Litvinchuk 等人使用脂质组学与免疫染色相结合,证明 ApoE 促进 9.5 月龄的 P301S 小鼠神经胶质细胞中胆固醇代谢和脂质积累的变化。LXR激动剂GW3965 饮食和 Abca1 过表达显着减少 9.5 月龄 P301S/ApoE4 小鼠的 tau 蛋白病、神经变性、突触损失和行为缺陷、神经炎症和神经胶质脂质积累。这些数据表明,促进神经胶质细胞脂质的流出可能改善 tau 蛋白和 ApoE4 相关神经变性,是一种潜在的治疗方法。

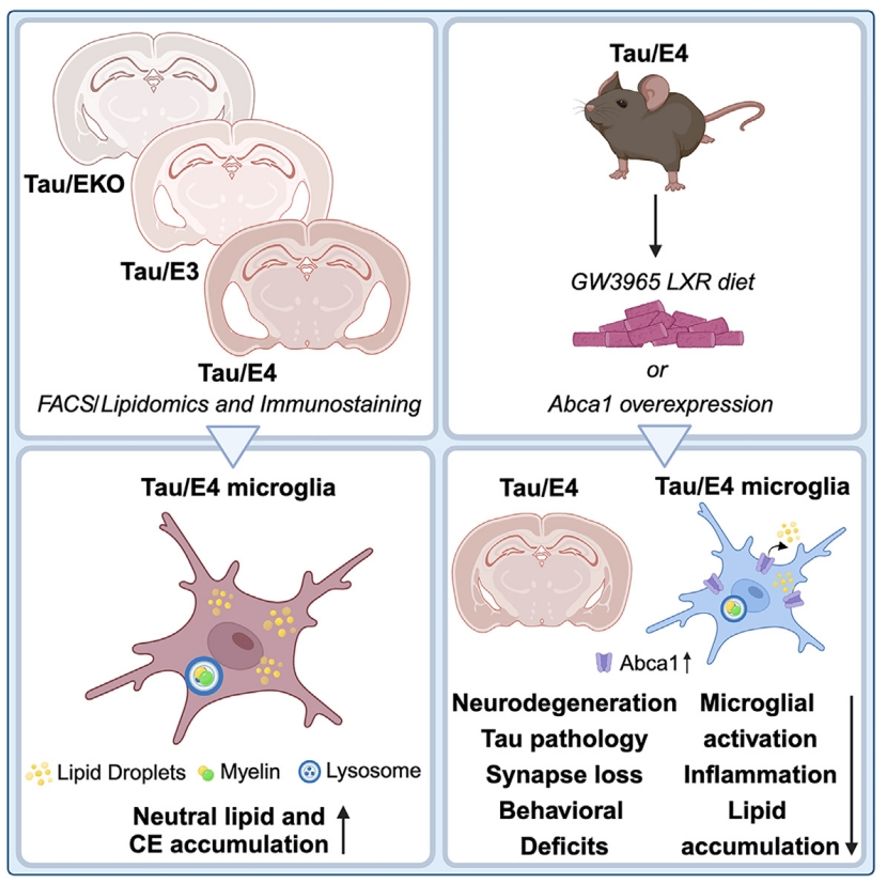

1. ApoE4对9.5月龄P301S小鼠前脑中胆固醇代谢的影响
首先,研究者通过对TE4小鼠进行脑区神经退行性变化的观察,发现其在海马、内嗅皮质和梨状皮质等脑区表现出明显的神经退行性变,并伴有比TE3小鼠心室增大。相比之下,TEKO小鼠在很大程度上避免了神经变性。此外,脂质组学分析揭示了ApoE4小鼠胆固醇代谢的紊乱,尤其在与tau依赖性相关的脂质类别中存在显著差异。研究者还进一步探究了tau蛋白病对不同ApoE亚型小鼠前脑脂质组的影响。结果显示,在9.5月龄时,TE4小鼠表现出多种脂质类别的显著变化,包括CE、BMP和LPC增加以及硫酸胆固醇和 4-β-羟基胆固醇的减少。这说明tau蛋白ApoE4之间存在强烈的相互作用,可能会协同导致TE4小鼠中观察到的胆固醇代谢受损、溶酶体脂质清除以及随后的神经炎症。(图一)
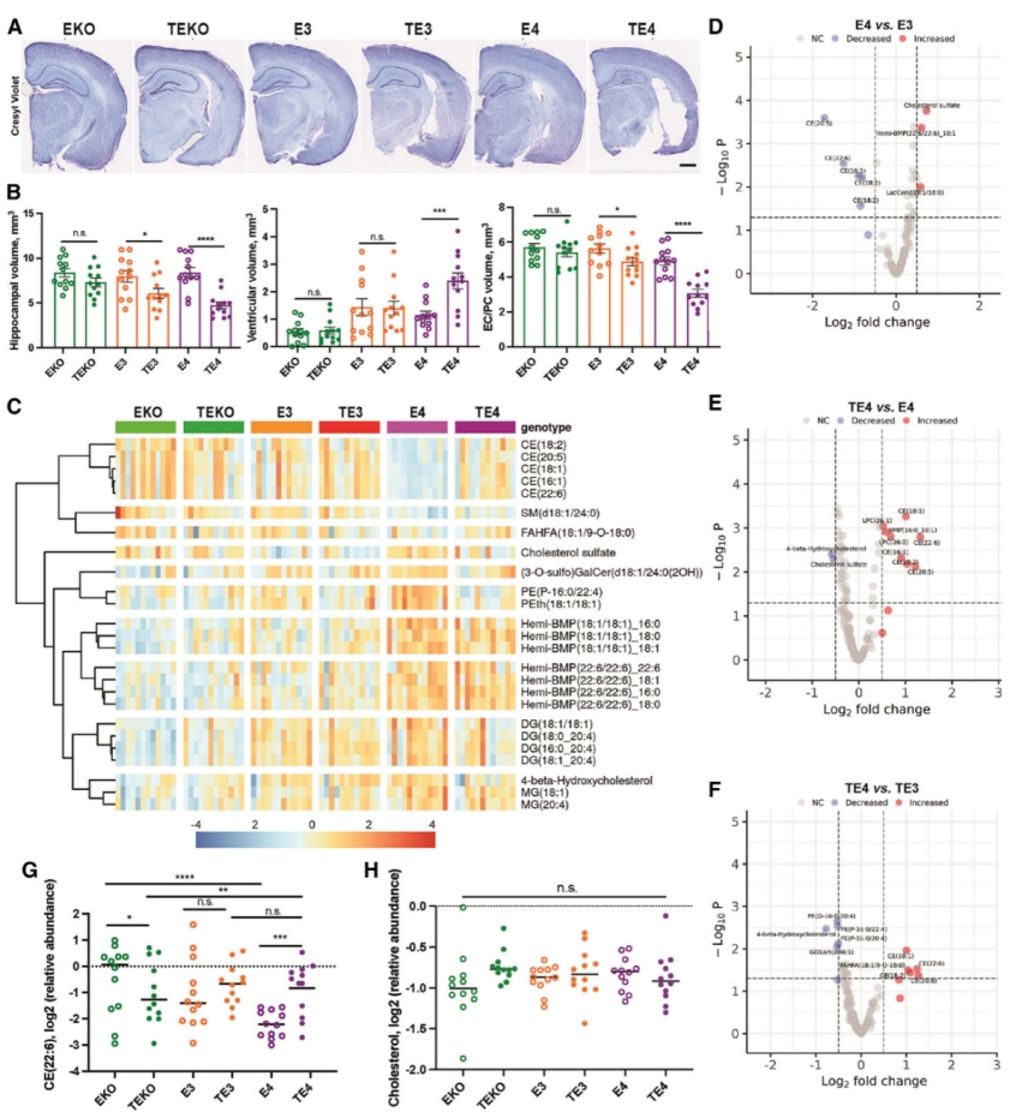
图一:ApoE4 诱导 9.5 月龄 P301S/ApoE KI 小鼠前脑胆固醇代谢变化
2. ApoE4诱导9.5月龄P301S小鼠胶质细胞中性脂质积累和胆固醇代谢的变化
为深入探究TE3、TE4和TEKO小鼠胶质细胞中的脂质积累模式,研究者使用BODIPY染色标记中性脂质,并以E06抗体染色氧化磷脂酰胆碱(oxPC)。在TE4小鼠的小胶质细胞中观察到显著的BODIPY+包涵体,这些信号主要分布在CD68+吞噬溶酶体内。结果表明TE4小鼠中神经胶质细胞发生脂质积累,尤其是中性脂质在溶酶体降解过程中受到损害。
此外,相对于E4小鼠,TE4小鼠的星形胶质细胞和小胶质细胞中CEs显著增加,而总胆固醇水平无显著变化。这表明TE4小鼠的小胶质细胞积累CE物质,可能解释了BODIPY+染色信号的增加。(图二)
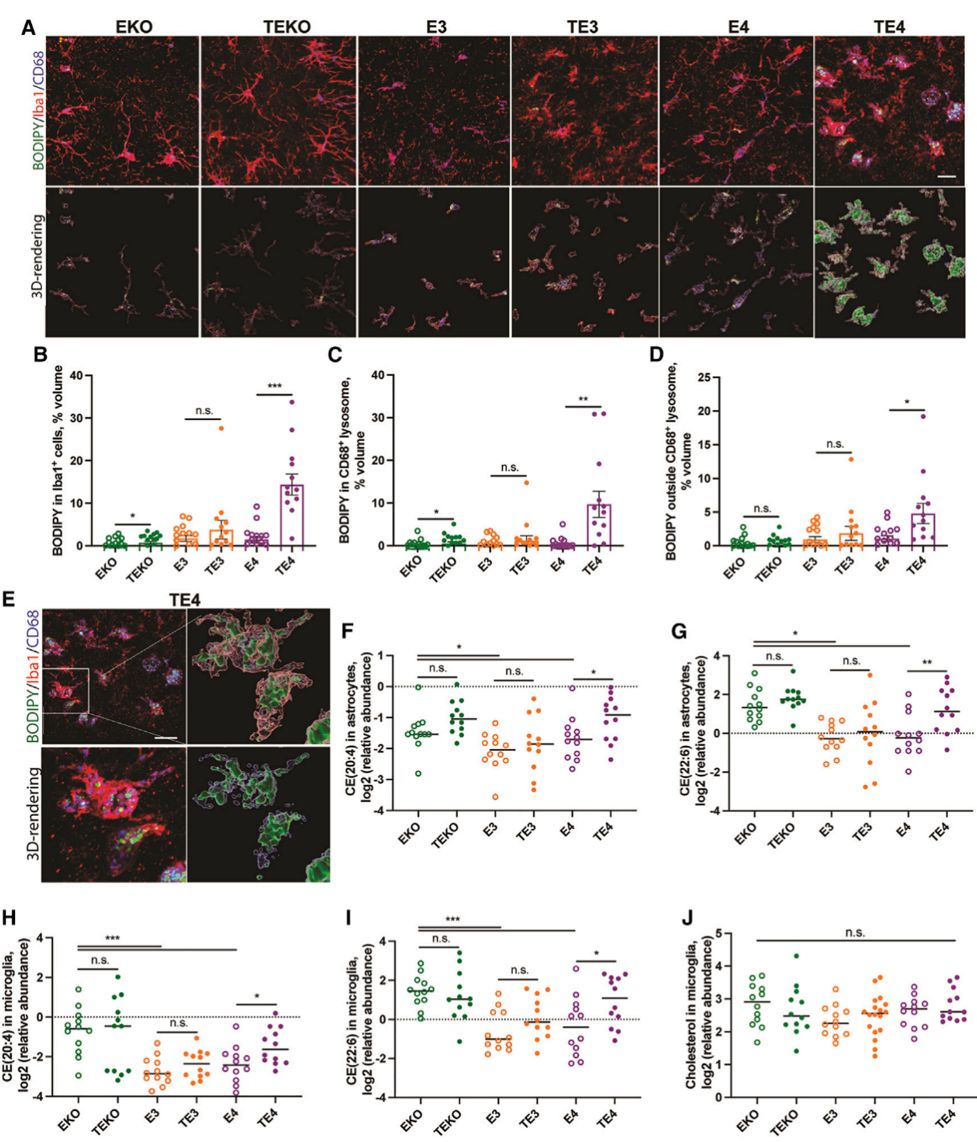
图二:ApoE4 诱导 P301S 小鼠神经胶质脂质积累
3. LXR激动剂GW3965诱导9.5月龄TE4小鼠脑中Abca1的表达,并可改善 9.5 月龄TE4 小鼠的神经退行性变、减少筑巢行为评分并降低磷酸 Tau 水平
神经胶质细胞中的脂质积聚与氧化应激和神经炎症反应增加有关,因此可能会促进神经退行性变。肝X受体(LXR)激动剂,这是一种实验性药物,可以降低细胞内的脂质水平。为了验证剂量和给药,作者用10 mg/kg的LXR激动剂GW3965治疗E4小鼠,作者观察到大脑中LXR靶基因Abca1 mRNA显著增加~1.5-2倍,同时Abca1蛋白增加~1.5-2倍。LXR激动剂的饮食对9.5月龄TE4小鼠产生了显著影响。该处理使得TE4小鼠的神经退行性变化减轻,体积减少、神经丝轻链水平下降,筑巢行为改善。同时,LXR激动剂治疗导致9.5月龄TE4小鼠病理性tau显著降低,而不影响ApoE水平。(图三)。
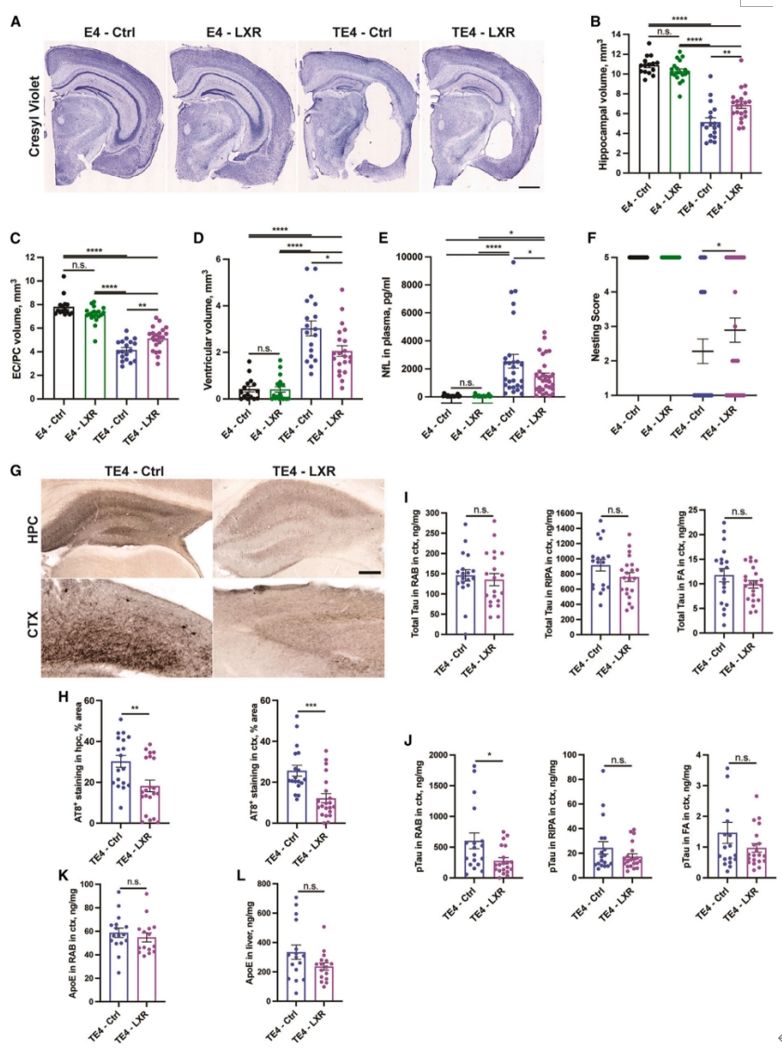
图三:LXR 激动剂 GW3965 可改善 9.5 月龄TE4 小鼠的神经退行性变、减少筑巢行为评分并降低磷酸 Tau 水平
4. LXR激动剂GW3965降低9.5月龄TE4小鼠的神经胶质反应性、T细胞浸润和炎症
在TE4小鼠中,神经胶质反应性在促进tau病理和神经变性中起着至关重要的作用。作者通过GFAP+染色区域量化和Iba1免疫染色评估了LXR激动剂对TE4小鼠胶质反应性的影响。结果显示,TE4-LXR小鼠相较于TE4-对照小鼠在hpc和ctx中GFAP+细胞数量减少。LXR治疗后,hpc中GFAP+细胞数量不变,但TE4小鼠的Iba1和CD68染色分别减少了50%和60%。这表明LXR激动剂显著抑制了TE4小鼠的胶质反应性,包括小胶质细胞和浸润巨噬细胞的活性。有趣的是,与TE4-对照小鼠相比,TE4-LXR小鼠的hpc和ctx中与疾病相关的小胶质细胞(DAM)相关的Clec7a降低,与TE4-LXR小鼠的hpc和ctx中与稳态小胶质细胞相关的P2ry12标志物显著增加。因此,LXR激动剂通过调节神经胶质细胞的整体特征,减少炎症反应,为神经保护提供了潜在机制(图四)。
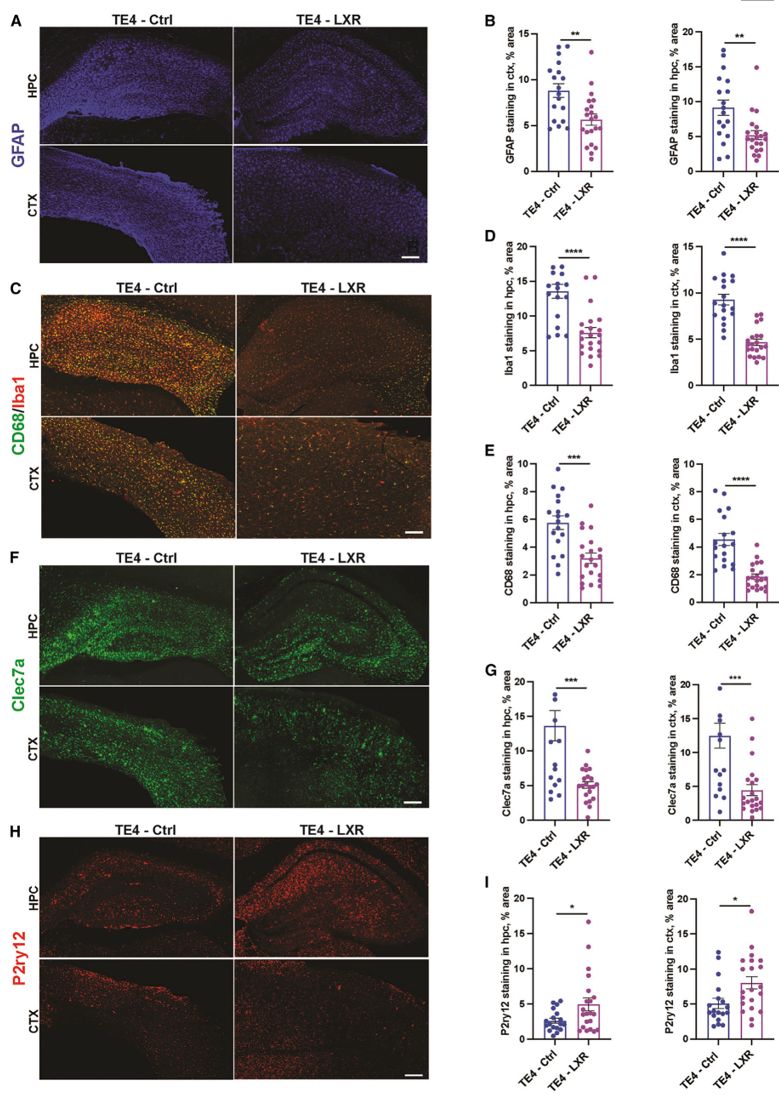
图四:LXR 激动剂 GW3965 减少 9.5 月龄TE4 小鼠的小胶质细胞和星形胶质细胞活化
5. LXR激动剂GW3965减少9.5月龄TE4小鼠突触丢失
在突触水平上,LXR激动剂的饮食显著减少了TE4小鼠CA3海马区的突触丢失。尽管TE4小鼠在对照组条件下表现出突触素染色的降低,但经过LXR激动剂处理后,突触素染色丧失程度显著减轻。共定位PSD95/突触素突触的增加也支持了LXR激动剂对突触功能的保护作用。进一步通过免疫染色,研究者观察到LXR激动剂减少了小胶质细胞对突触物质的吞噬,从而减缓了突触的降解。总之,这些结果表明LXR激动剂饮食可以保护TE4小鼠免受小胶质细胞介导的突触丧失(图五)。
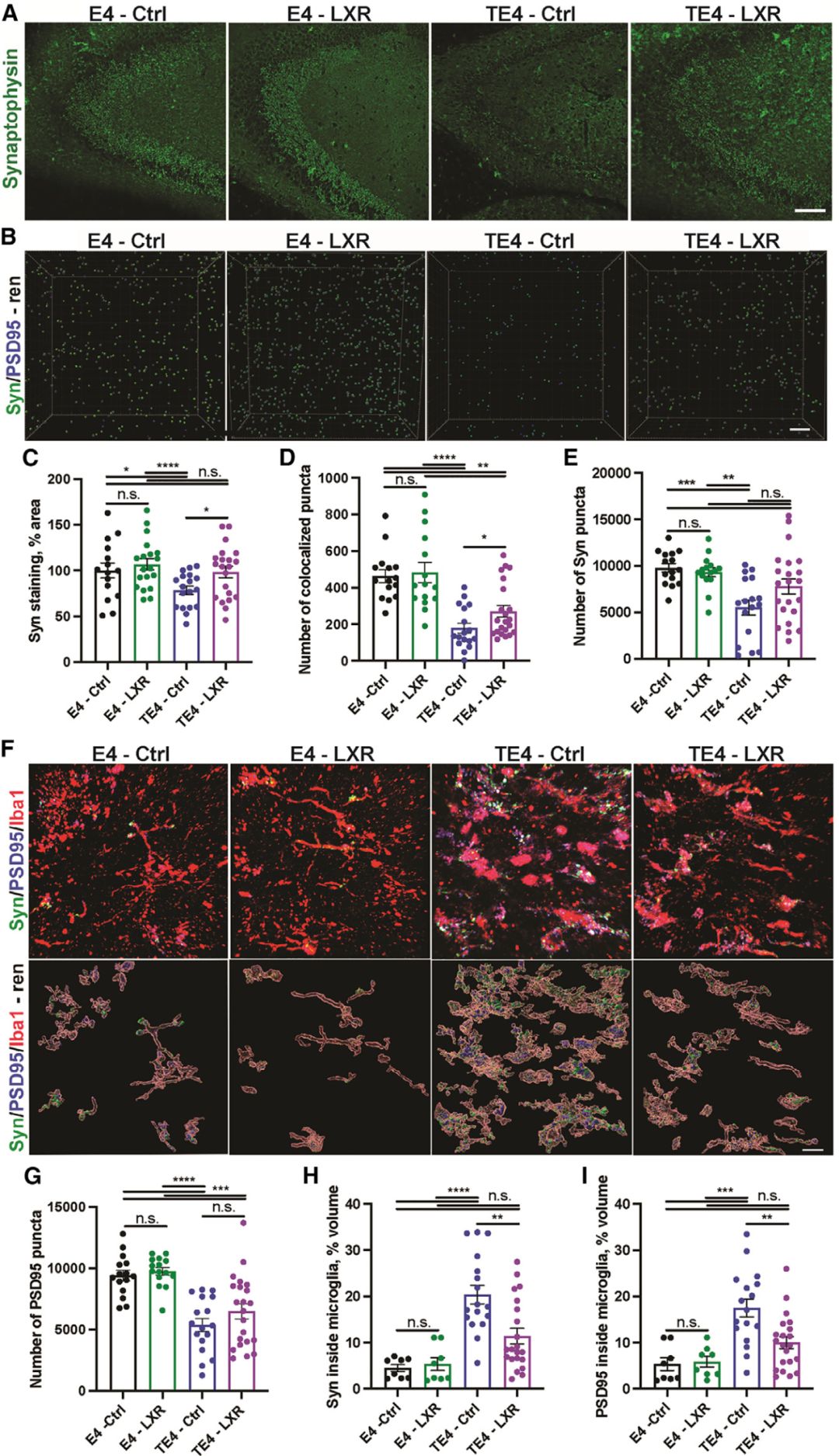
图五:LXR 激动剂 GW3965 减少 9.5月龄TE4 小鼠的突触损失
6. 9.5月龄TE4 小鼠中的 LXR 激动剂在基因表达水平上诱导炎症反应和胆固醇代谢的变化
作者通过RNA测序和WGCNA分析了LXR激动剂对E4和TE4小鼠海马组织的影响。结果显示TE4-LXR小鼠与TE4-对照小鼠相比,在转录水平上存在显著差异,涉及多个功能通路,包括免疫反应、胆固醇代谢和生物合成途径。WGCNA分析揭示了一个与LXR激动剂正相关的模组,与TE4-LXR组呈正相关,与TE4-对照组呈负相关。该模组中的基因主要参与胆固醇代谢和生物合成、甲戊酸途径、LXR和SREBP1途径以及蛋白酶体降解。基因表达谱图谱和细胞类型聚类显示,TE4-LXR小鼠中LXR/SREBP转录程序的激活主要通过调节星形胶质细胞和小胶质细胞中的胆固醇代谢和生物合成,以及通过诱导神经元细胞和OPC/少突胶质细胞中的神经元代谢、突触功能和蛋白酶体降解来发挥作用。(图六)
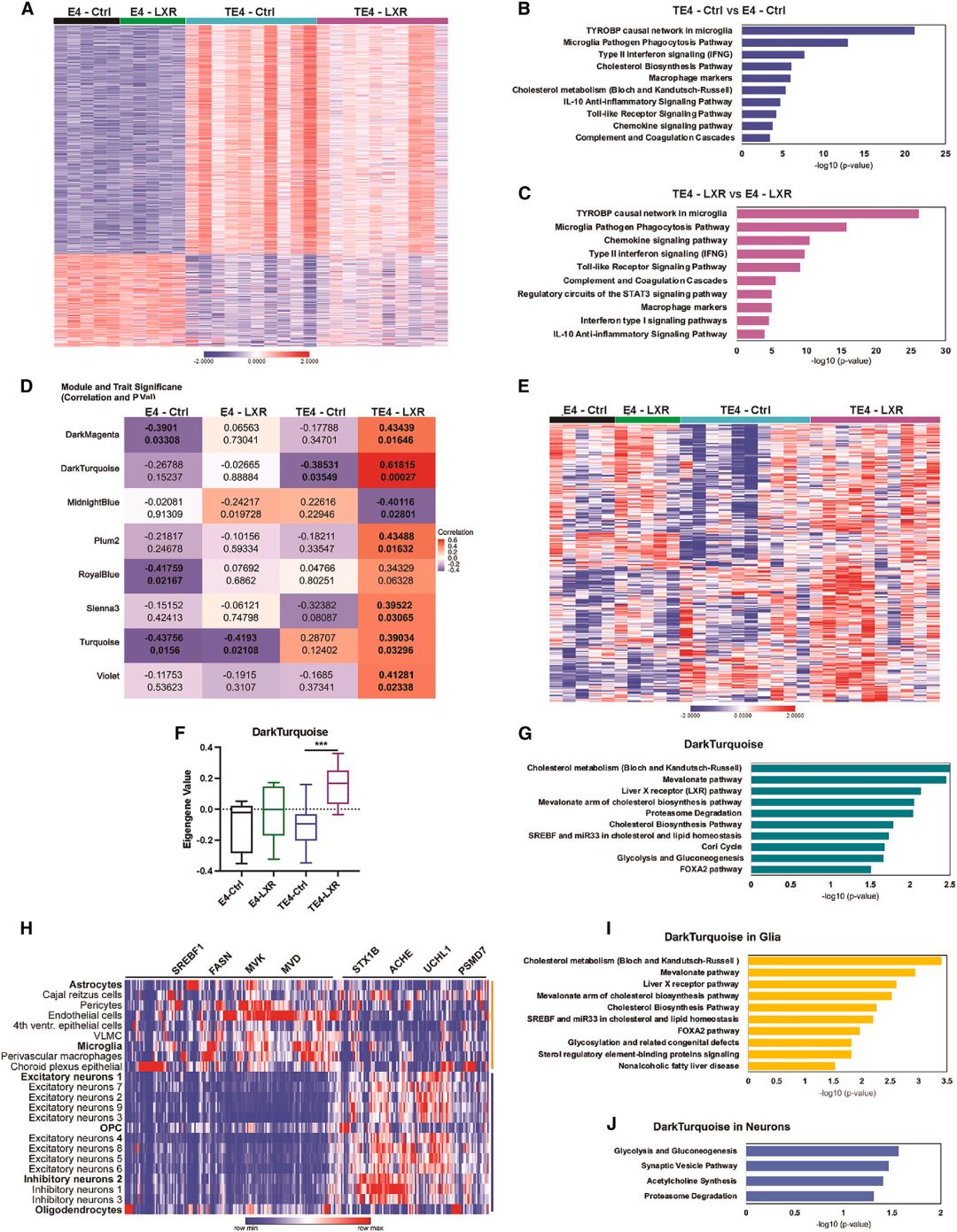
7. LXR激动剂GW3965减少9.5月龄TE4小鼠的脂质积累
作者通过无偏倚脂质组学测试发现,LXR激动剂对TE4小鼠的脑脂质谱产生显著影响。在E4和TE4小鼠的前脑中,多种脂质如CE、BMP、脂肪酸、甘油脂和氧化固醇呈现明显变化。比较TE4-Ctrl和E4小鼠,证实了ApoE4存在时P301S小鼠的胆固醇代谢受损、溶酶体功能障碍和炎症。LXR激动剂诱导TE4小鼠中脂肪酸和BMP的显著增加,同时减少了胆固醇和氧化固醇。此外,LXR激动剂治疗后,多种CE类型的显著下降,与CE在TE4-Ctrl小鼠中的升高相对应。WGCNA分析显示,LXR激动剂治疗小鼠的前脑CE与血浆NfL水平显著相关,表明NfL/神经变性与大脑中CE积累密切相关。最终,BODIPY染色结果表明,通过LXR激活增加TE4小鼠的胆固醇外排,可以减少大脑和小胶质细胞中的中性脂质积累,从而具有潜在的神经保护作用。(图七)
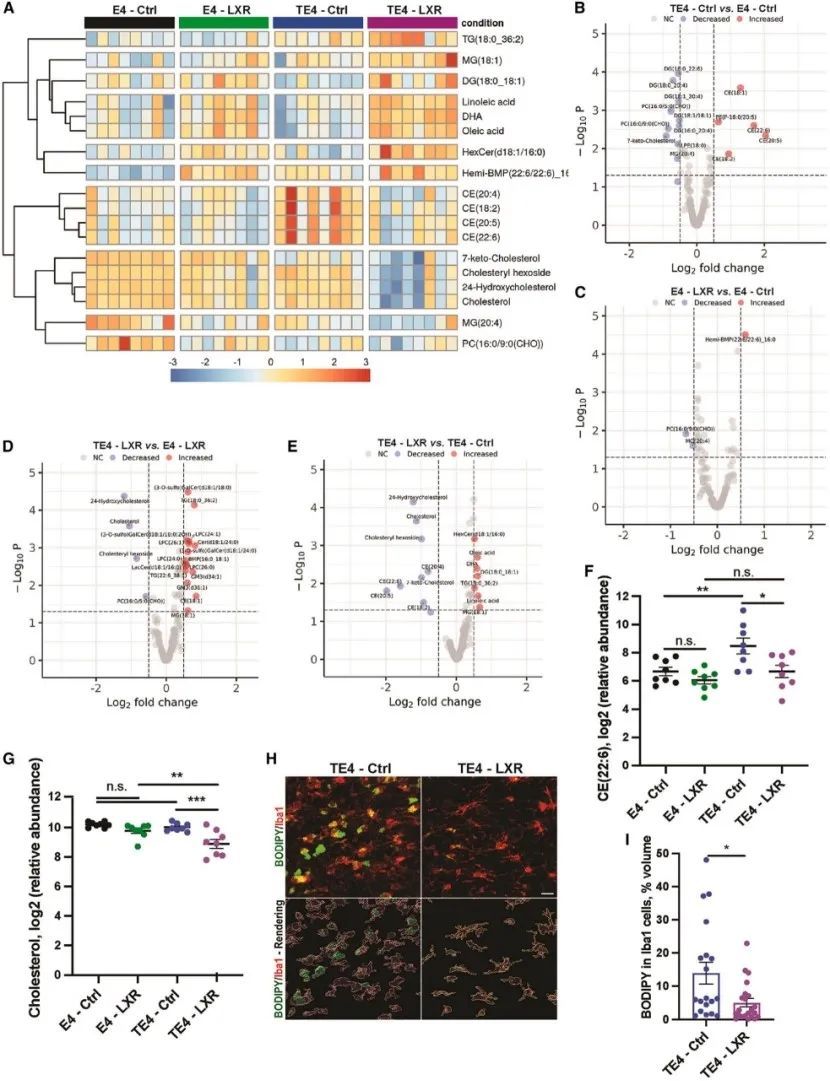
8. 在9.5月龄TE4小鼠中,Abca1过表达可减少神经退行性变、tau病理、小胶质细胞激活和脂质积累
作者在研究中将TE4小鼠与过表达Abca1的转基因小鼠进行脑内杂交,发现Abca1/E4小胶质细胞表达Abca1水平明显高于非Abca1转基因小胶质细胞。对比TE4小鼠,9.5月龄TE4/Abca1小鼠对海马和EC/PC的萎缩具有显著的保护作用,伴随着脑神经退行性变减少、血浆中NfL蛋白水平下降和筑巢行为测试功能的改善。评估Abca1过表达对tau病理的影响,发现TE4/Abca1小鼠hpc和ctx中AT8染色显著降低,同时小胶质细胞/巨噬细胞免疫反应性和脂质积累减少。综上,Abca1过表达在TE4小鼠中显著保护免受神经变性、tau病理、小胶质反应性和脂质积累,效果类似于LXR激动剂GW3965饮食。(图八)
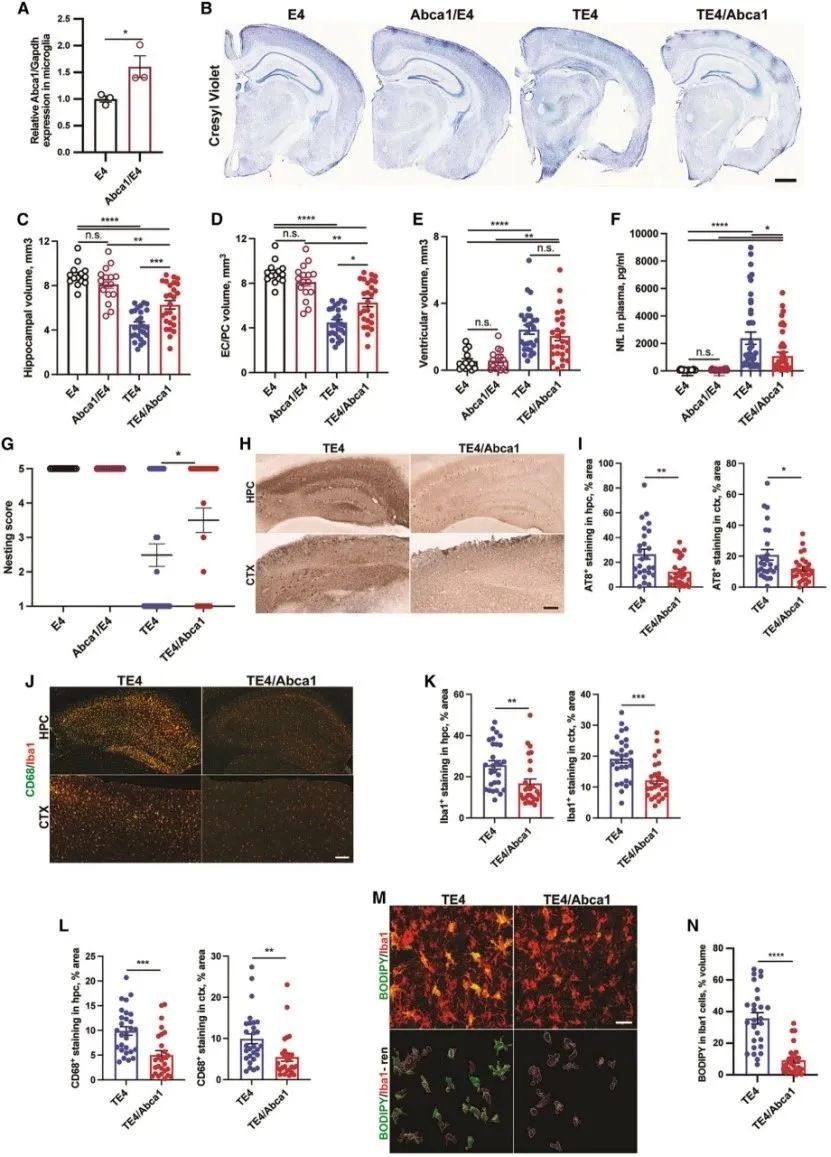
图八:Abca1过表达改善9.5月龄TE4小鼠的神经变性和tau病理,降低小胶质/髓样细胞的反应性和脂质积累
总结
作者利用靶向脂质组学结合免疫染色,在9.5月龄的P301S-tau转基因小鼠中,用人源性ApoE3(TE3)或ApoE4(TE4)靶向取代小鼠ApoE,以及在缺乏ApoE(TEKO)的小鼠中,解析ApoE亚型在调节胶质细胞脂质代谢中的作用。作者证明,ApoE4的表达诱导P301S小鼠前脑和小胶质细胞中CEs的显著升高,并增强小胶质细胞内BODIPY+中性脂质的积累。肝X受体(LXR)激动剂GW3965或Abca1过表达治疗可减少TE4小鼠的tau病理学和相关的神经退行性变、神经胶质炎症和突触缺陷。
原文链接:
https://doi.org/10.1016/j.neuron.2023.10.023
参考文献
Litvinchuk A, Suh JH, Guo JL, Lin K, Davis SS, Bien-Ly N, Tycksen E, Tabor GT, Remolina Serrano J, Manis M, Bao X, Lee C, Bosch M, Perez EJ, Yuede CM, Cashikar AG, Ulrich JD, Di Paolo G, Holtzman DM. Amelioration of Tau and ApoE4-linked glial lipid accumulation and neurodegeneration with an LXR agonist. Neuron. 2023 Nov 16:S0896-6273(23)00804-8. doi: 10.1016/j.neuron.2023.10.023. Epub ahead of print. PMID: 37995685.
编译作者:欢欢熊吧(brainnews创作团队)
校审:Simon(brainnews编辑部)


