未来CAR-T治疗的新思路:优化T细胞亚群的特性来提高治疗效果

01介绍
细胞免疫疗法,如CAR-T,一种使用表达靶向肿瘤抗原的基于抗体的嵌合抗原受体的T细胞的疗法,是针对不同类型的血液恶性肿瘤以及实体癌的有效疗法。
CAR-T(最初称为T体)是指表达抗原特异性或基于抗体的嵌合受体的T细胞,具有抗体特异性和T细胞效应子或调节功能,由Eshhar和他在以色列魏茨曼科学研究所的同事于20世纪80年代首次描述。
CAR结合了抗体的单链可变片段(scFv),驱动针对肿瘤抗原的特异性。一旦CAR-T结合肿瘤抗原,T细胞增殖和扩增被激活,T细胞细胞毒性功能导致肿瘤细胞死亡。
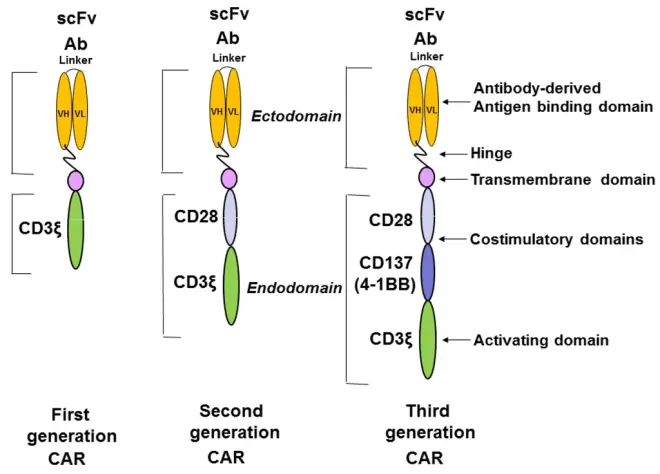
图1嵌合抗原受体构建体的结构,显示了第一代、第二代和第三代CAR结构。第一代汽车只有一个激活域,第二代CAR有一个激活域和一个共刺激域,第三代CAR有一个激活域和两个共刺激域。
最近的多项研究强调了在CAR-T细胞免疫疗法中,分析T细胞亚群的功能和个体患者的T细胞谱之间的差异的重要性。
T细胞亚群的多个方面,包括:CD4+和CD8+细胞亚群和分化;记忆和效应T细胞功能;细胞外T细胞标记物;T细胞的遗传、表观遗传和代谢信号通路。作用于CAR-T细胞免疫治疗中,提供改善CAR-T免疫治疗的前景。
02CD4和CD8细胞亚群
T细胞在胸腺中成熟,表达TCR (T细胞受体),在其表面表达CD8蛋白,称为CD8+T细胞(细胞毒性),在表面表达CD4蛋白的被称为CD4+T细胞(辅助T细胞)。
2.1CD4+细胞亚群
CD4+细胞分化成不同的亚群:Th1、Th2、Th9、Th17、Th22、Treg(调节性T细胞)和Tfh(滤泡辅助性T细胞),如图2所示 。

图2不同的CD4+t细胞亚群。不同的CD4+不同的细胞因子从初始T细胞产生亚群,每个CD4+亚群产生不同类型的白细胞介素。
Th1细胞:
Th1细胞参与细胞免疫应答以及抵御病原微生物感染,包括促进细胞毒性T细胞的增殖分化,促进巨噬细胞的吞噬功能。Th1细胞的特征性转录因子为T-bet,分泌IL-2, IFN-γ, TNF-α, LT-α。Th1的促炎特性使其具有清除病原微生物和抗肿瘤免疫力,但是另一方面Th1和IFN-γ会导致炎症性疾病(如炎症性肠病)和自身免疫性疾病(如I型糖尿病和类风湿关节炎)。
Th2细胞:
Th2细胞参与体液免疫应答以及抵御寄生虫感染,包括促进B细胞增殖分化为浆细胞,产生抗体。Th1细胞的特征性转录因子为GATA3,分泌IL-4、IL-5、IL-6、IL-10、IL-13等细胞因子。过度的Th2反应与过敏和哮喘有关。
Th9细胞:
Th9是一类辅助性T细胞,在抵御细胞外寄生虫方面发挥作用。Th9分泌大量的IL-9和IL-10。新的研究发现Th9与肿瘤进展有关,可能发挥抗肿瘤和促肿瘤双重作用,Th9也与某些炎症性疾病的发生和发展有关。
Th17细胞:
Th17细胞参与炎症应答和抵御胞外病原微生物(尤其是在肠道、呼吸道黏膜)。Th17细胞的特征性转录因子为RORγt,分泌IL-17A、IL-17F、IL-21、IL-22和IL-26。Th17与多种自身免疫性疾病有关,如多发性硬化症、类风湿性关节炎,银屑病,炎症性肠病等。
Th22细胞:
Th22是一类参与皮肤免疫的辅助性T细胞,分泌IL-22、不产生IL-17,表达芳香烃受体(ARH)和CCR10。Th22与多种自身免疫性疾病有关,如包括类风湿性关节炎、系统性红斑狼疮、银屑病、多发性硬化等。
Tfh细胞:
Tfh(滤泡辅助性T细胞)辅助B细胞在生发中心的存活与增殖,促进B细胞向浆细胞分化、抗体类别转换和抗体亲和力成熟。Tfh表达Bcl-6和CXCR5。
Treg细胞:
Treg(调节性T细胞)是一类可对免疫应答进行负调控的细胞,其最突出的功能是维持自身耐受和免疫稳态。Treg根据起源可分为nTreg(自然调节性T细胞)和iTreg(诱导型调节性T细胞)。Treg表达CD25、Foxp3,低表达或不表达CD127。Treg的功能异常会导致多种自身免疫和炎性疾病。
2.2CD8+细胞亚群
CD8+细胞随着分化,形成不同亚群,显示在下图3。

图3 CD8的分化细胞亚群:TN幼稚T细胞,TSCM记忆T细胞,TCM中央记忆T细胞,TEM效应记忆细胞,TEFF效应T细胞。
TN细胞:
TN细胞是指未经分化的幼稚T细胞,通常是在胸腺内产生的并且在进入外周血液系统之前,这些细胞还不具备抗原特异性,尚未接受信号转导和增殖,无法进行深刻的免疫反应。TN细胞通常表达CD45RO的低水平,CD27 / CD28。它们的关键作用是为后续的T细胞分化和进化做好准备。
TSCM细胞:
TSCM细胞是一个全新的、相对成熟的T细胞亚群,有称之为“免疫记忆一级细胞(Immunological Memory Stem cells)”。TSCM细胞表现出中等至高强度的表面CD45RA和CD62L,同时也表达了干细胞标记物CD34和CD133。TSCM细胞有着高度的自我更新和自我扩增能力,以及良好的免疫记忆能力。它们可以在长时间内维持着多能性,随着身体的需要进化为TCM、TEM、T effector和TN细胞。
TCM细胞:
TCM细胞是中央记忆T细胞,这类细胞主要存在于淋巴结和脾脏中。TCM细胞是具有记忆性的CD45RO、CD62L的T细胞亚群,其免疫学特征是表达CD62L / CCR7受体,是长期外周循环的T细胞记忆池,在淋巴结中发挥重要作用,能够快速定位全身各处的免疫受体抗原(antigen receptors)。
TEM细胞:
TEM细胞是效应性记忆T细胞的重要组成部分,这类细胞是CD45RO高表达的T细胞,具有表面CD95、CD122、CD44、CXCR3、CCR5、CD11a、CD2、CD8α等特点。TEM细胞比TCM更容易穿过组织障壁,有着强大的迁移和栖息能力,特别是有较高的直接杀伤作用,从而有效对抗病原体。
TEFF细胞:
T效应细胞是免疫系统最主要的细胞类型之一,主要负责发挥炎症反应和抗原特异性的功能。TEFF细胞被激活后,会立即向外分泌各种细胞因子,如细胞因子、趋化因子等,引起炎性细胞浸润和伤害。
03不同T细胞亚群的作用
CAR-T疗法是针对血液系统恶性肿瘤的非常有效的免疫疗法,面临的挑战之一是如何设计T细胞,使其对Treg细胞具有抗性,并抑制抗肿瘤信号传导,并增加T细胞效应子和记忆功能,以增强抗肿瘤免疫反应。
因此我们需要分析和研究个体患者的CD4/CD8比率及其亚群的T细胞谱,目的是改善效应细胞和记忆功能,增加T细胞的持久性,以进行有效的CAR-T细胞治疗。
有多个途径可以提高CAR-T细胞治疗效果(如图4),包括有:

图4提高CAR-T细胞治疗效果的不同潜在途径
PART.1
选择不同的T细胞亚群,寻找个体化的T细胞谱。根据患者的T细胞亚群分析,选择最适合的T细胞亚群来制作CAR-T细胞。例如,在B细胞淋巴瘤患者中,CD8+ T细胞相对较少,因此需要使用CD4+ T细胞。
PART.2
增加对Treg细胞的抑制。Treg细胞可以抑制有效的免疫应答,因此通过选择破坏Treg细胞的CAR-T细胞,可以提高治疗效果。
PART.3
抑制免疫检查点,如PD-1和CTLA-4,可增强免疫应答,从而提升疗效。这是现代免疫治疗的常用策略,可以增强CAR-T细胞杀菌作用,同时减少其在体内的耐药性。
PART.4
调整T细胞代谢,可以增强细胞的存活能力、杀伤能力和治疗效果。例如,在制作CAR-T细胞时,添加一些细胞增殖因子和抗氧化物,可以延长CAR-T细胞的寿命,同时提高其杀伤基因改造的靶细胞的能力。
PART.5
不同细胞因子和共刺激CAR结构域的组合可用于增加CAR-T细胞治疗的功效。例如,通过结合CD28和4-1BB结构域,可以增强CAR-T细胞的存活和杀伤基因改造的靶细胞的能力,同时减少CAR-T细胞的表观耗损。
另外特别需要考虑的方面是,由于患者的T细胞谱与健康人的不同,并且在患者之间有所不同,这表明需要个体化的T细胞亚群谱和个体化的免疫治疗来有效治疗癌症。
04结论和展望
上文显示了T细胞分化的复杂性。
由于CAR-T疗法核心就是从从癌症患者血液中提取出用于扩增的T细胞,因此应当分析CD4/CD8的比率,以及记忆标记物如CD45RA、CD45RO和其它标记物如CD26、CD95、CCR-7和CD62L,以选择不同比率的不同T细胞亚群,在临床试验中进行研究,以获得更有效和个性化的治疗。
应分析分选的CD4或CD8细胞群和T细胞亚群,它们具有特定的记忆或干细胞记忆标记以及遗传、表观遗传和代谢特征,并结合免疫检查点抑制剂,用于调节CAR-T治疗的疗效。
只有这样,才能在未来更有效地寻找并制备出临床最佳CAR-T。
*内容为【干细胞精研社】原创,转载请注明来源
图片来源于网络,侵删

