玩转Sanger测序仪丨专题五:HPV E6/E7 DNA 全分型核酸检测
人乳头瘤病毒(HPV)
人乳头瘤病毒(Human Papilloma virus,HPV)是一种小型无包膜的双链环状DNA病毒。HPV具有嗜上皮特性,可以感染人体皮肤黏膜任何部位,引起皮肤黏膜角质形成细胞的过度增殖,HPV与多种癌症的发生有关。
HPV基因组序列存在10%以上的不同,即为不同的基因型别。目前已发现超过200种型别的HPV,按HPV生物学性和致癌性,可将HPV为低危型(LR-HPV)与高危型(HR-HPV)。LR-HPV会引起人表皮良性赘生物(如尖锐湿疣、寻常疣等),而HR-HPV可引起宫颈上皮病变和阴道病变等,更可进展为皮肤鳞癌、生殖器恶性肿瘤(如子宫颈癌、阴道癌、外阴癌、肛门癌、阴茎癌、头颈部癌等)。
HPV的传播途径主要为性传播,还有母婴传播和皮肤黏膜接触等。

人乳头瘤病毒(HPV)与宫颈癌
1976年德国科学家Hausen提出HPV与宫颈癌的病因关系的假设。后大量的流行病学研究印证了Hausen的理论,即高危型HPV持续感染是子宫颈癌的致病“元凶”。
1 宫颈癌流行病学
宫颈癌是全球关注的女性恶性肿瘤,2020年全球宫颈癌新发60.4万例,死亡约34.2万例,是全球女性常见的第四大恶性肿瘤。
根据世界卫生组织(WHO)国际癌症研究署(IARC)的统计,2020年我国子宫颈癌新发病例和死亡病例约为11万和5.9万例,分别占全球新发病例和死亡病例的18%和17%。近年来,我国加强了宫颈癌的防治工作,推进实施三级预防策略,仍面临以下主要问题:
(1)宫颈癌筛查覆盖率较低;
(2)细胞学检查存在灵敏度低、结果具有主观性、质量难以保证等问题,但目前仍是宫颈癌筛查的主要方法;
(3)HPV核酸检测技术具有灵敏度高、可重复性高等特点,相较于细胞学检查可检出更多的宫颈癌和癌前病变,但尚未在我国宫颈癌筛查项目中广泛使用。


2 中国子宫颈癌女性的高危型HPV呈现多样性
2021年WHO发布的《预防宫颈癌:宫颈癌前病变筛查和治疗指南》中指出HR-HPV检测通常包括14种型别:HPV16、18、31、33、35、39、45、51、52、56、58、59、66、68型。而中国人最常见致病高危型有16、18、31、33、39、45、51、52、56、58、59等,远不止16/18。

图源:孟俊, 许啸声,陆一一, 范臻佳,蔡刚.2017年至2020年上海地区妇女宫颈脱落细胞 HPV 感染亚型调查分析[J].诊断学理论与实践, 2021,20(6):567-571.
3 高危型HPV持续性感染导致宫颈癌
HPV基因组可分为3个区域:早期基因(包含开放阅读框E6、E7、E1、E8、E2、E4、E5)、晚期基因(包含开放阅读框L1和L2),以及非编码上游调节区(URR)又称为长控制区(LCR)(图1),各基因的功能和特点如下(表1)。


初始HPV感染(潜伏期):
HPV以游离的环状DNA状态存在,处于低拷贝水平复制,此时细胞高级别病变风险低;
持续HPV感染(活跃期):
HPV基因与人基因组发生DNA整合,发展为持续性感染,导致宫颈上皮内瘤样病变(CIN I/II/III)甚至演变为浸润癌。

HPV感染宫颈上皮后,因其基因型别不同、是否持续感染及持续感染时间不同,其致病风险也显著不同。因此,对HPV进行分型检测并明确是否存在持续感染具有重要的临床意义。
HPV检测方法
1 HPV检测:从细胞学检测时代进入HPV核酸检测时代
从HC2检测到L1 DNA检测,再到HPV E6/E7 基因分型检测,HPV核酸检测技术的发展为宫颈癌筛查领域带来了里程碑式的变革。以致癌基因(E6/E7)为靶点的检测产品上市,标志着宫颈癌的筛查将能够避免晚期病变患者因L1丢失而造成漏检,且全分型检测对于中高危型别持续感染的癌变风险系数提供了更有价值的临床评估手段。

2 L1区检测还是E6/E7区检测?
研究发现,宫颈上皮细胞从低级别病变发展为高级别病变或癌变的过程中,HPV 基因组通常会发生整合,整合过程中,L1 DNA可能丢失,但E6/E7 DNA持续存在。
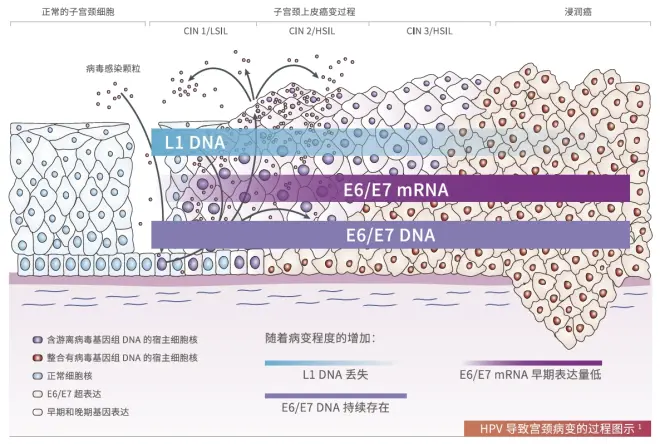
国外研究 1
2013年于《欧洲妇产科学和生殖生物学》上发布的《宫颈癌症筛查:应使用哪种HPV检测,L1或E6/E7?》研究综述中提到:在宫颈从低级别病变发展为高级别病变或浸润性宫颈癌的过程中,HPV基因组会发生整合。在整合的过程中,L1基因会丢失,但E6/E7基因始终存在。如果HPV病毒基因组发生完全整合,那么以L1基因作为靶点的HPV检测方法会漏检宫颈癌/癌前病变;而以E6/E7基因作为靶点的HPV检测方法不会造成漏检。

国外研究 2
一项基于 15774 例病人样本的研究发现,跟型别特异性 E6/E7引物 PCR 比较,基于L1基因设计的通用引物MY 09/11 PCR 检测会造成 10.9%(522例)的漏检:409 例由 MY09/11PCR 检测结果为阴性的病人中,随访发现最终有104人(25.4%)发展为 CIN2+。
在4771例HPV阳性标本中,以L1作靶点与E6/E7作靶点相比,各个HPV型别的漏检情况如下:

国内研究
王慧静等人选择高危型 (HR)-HPV16 亚型的 E6/E7 区基因和 HR-HPV 的 L1 区基因设计特异性引物,建立高危型 HPV16 分型检测方法,分别收集宫颈组织(慢性宫颈炎,宫颈上皮内瘤变CIN1/2/3、宫颈鳞癌)76 例标本,采用新建立的方法对 HPV 早、晚期基因进行 PCR检测,同时与杂交捕获二代法 (HCⅡ) 检测的 HPV L1 基因进行比较。
结果显示:E6/E7 基因 HPV16 分型检测阳性率为 55.3%,HPV L1 和 HCⅡ-HPV L1 检测阳性率均为 25.0%,E6/E7 基因阳性率明显高于 HPV L1 和HCⅡ-HPV L1,差异有统计学意义 (P<0.01)。HPV E6/E7基因比 L1 基因检测更具灵敏、高效、实用的特点,将E6/E7基因检测与病理诊断结果相结合,可作为预测评价临床早期宫颈病变基宫颈癌的有效方法。

《加速消除宫颈癌行动计划(2023-2030年)》

为贯彻落实《“健康中国2030”规划纲要》和《中国妇女发展纲要(2021-2030年)》,积极响应世界卫生组织提出的“加速消除宫颈癌全球战略”,加快我国宫颈癌消除进程,国家卫健委制定了《加速消除宫颈癌行动计划(2023-2030年)》,着重提出了加速消除宫颈癌行动的主要目标:
完善体系
进一步完善宫颈癌防治服务体系,提高综合防治能力,构建社会支持环境,努力遏制宫颈癌发病率、死亡率上升趋势,减轻宫颈癌社会疾病负担。
到2025年
· 试点推广适龄女孩HPV疫苗接种服务;
· 适龄妇女宫颈癌筛查率达到50%;
· 宫颈癌及癌前病变患者治疗率达到90%。
到2030年
· 持续推进适龄女孩HPV疫苗接种试点工作;
· 适龄妇女宫颈癌筛查率达到70%;
· 宫颈癌及癌前病变患者治疗率达到90%。
HPV检测解决方案
人乳头瘤病毒(HPV)基因检测及分型检测试剂盒(PCR-毛细电泳片段分析法)以E6/E7 DNA为靶点的25种HPV全分型检测解决方案,涵盖18种中高危型和常见可引起尖锐湿疣的低危型,助力加速消除子宫颈癌全球战略,为适龄妇女提供宫颈癌筛查服务,促进宫颈癌早诊早治,提高妇女健康水平。
检测原理
采用多重 PCR 和毛细电泳技术,针对 HPV 基因组的早期表达基因 E6、E7、E1 设计特异性引物,对不同 HPV 型别的基因进行特异性扩增及毛细电泳分离,根据特异性扩增片段长度的不同在一次检测中对 25 种 HPV 型别同步进行分型。
检测靶点
● 18种中高危型:16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82
● 7种低危型别:6, 11, 42, 43, 44, 81, 83*覆盖WHO在2021年发布的《预防宫颈癌:宫颈癌前病变筛查和治疗指南》中指出HR-HPV检测通常包括14种型别:HPV16、18、31、33、35、39、45、51、52、56、58、59、66、68型。
检测流程
采样→核酸自动化提取→普通PCR→毛细管电泳分析
结果意示
双重质控,保障实验过程和样本有效性
检测优势
● 以致癌基因 E6/E7 DNA为检测靶点,相比L1减少约10%高级别病变中的漏检;
● 25种HPV型别全分型,对高危型别持续感染的风险随访提供更有价值的评估手段;
● 毛细电泳片段分析法,单管多重技术、双重质控和防污染体系,提供更简易精准的HPV筛查手段。
参考文献及资料
[1] Vaccine前沿丨一文解读HPV作用机制与最新动态!(https://mp.weixin.qq.com/s/SDNherq3DINMauZ5ARzy4w)
[2] ICO HPV Information Centre. Human Papillomavirus and Related Diseases Report. China, 2018.
[3] Globocan:国际癌症研究中心(IARC)统计全球185个国家/地区的36种癌症发病率、死亡率以及癌症发展趋势等相关数据的数据库;ICO: Information Centre on HPV and Cancer.
[4] Bruni L, Albero G, Serrano B, Mena M, Collado JJ, Gómez D, Muñoz J, Bosch FX, de Sanjosé S. ICO/IARC Information Centre on HPV and Cancer (HPV Information Centre). Human Papillomavirus and Related Diseases in China. Summary Report 22 October 2021.
[5] 孟俊, 许啸声,陆一一, 范臻佳,蔡刚.2017年至2020年上海地区妇女宫颈脱落细胞 HPV 感染亚型调查分析[J].诊断学理论与实践, 2021,20(6):567-571.
[6] 《WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, second edition》
[7] 人乳头状瘤病毒核酸检测用于宫颈癌筛查中国专家共识(2022).中华医学杂志2023.
[8]Woodman C B, Collins S, Y oung L S, et al. The natural history of cervical HPV infection: unresolved issues[J]. Nature Reviews Cancer, 2007, 7(1): 11-22.
[9]W.A.A. Tjalma et,al. Cervical cancer screening:which HPV test should be used-L1 or E6/E7?European Journal of Obstetrics & Gynecology and Reproductive BioLogy170(2013)45-46.
[10]Comparison of MY09/11 consensus PCR and type-specific PCRs in the detection of oncogenic HPV types. Journal of Cellular & Molecular Medicine,2007,11(4):881-891.
[11]王慧静,谢旺凯,王俭,等.HPV E6/E7基因和HPV L1基因DNA检测的比较及意义[J].中外医学研究, 2016.
[12]《人乳头瘤病毒(HPV)核酸检测及基因分型、试剂技术审查指导原则》

