【热点题型】新情境下的陌生氧化还原方程式书写与配平|适合高二与高三同学学习-高一

杰哥 | 新情境下的陌生氧化还原方程式书写与配平

1️⃣2023·北京卷
以银锰精矿(主要含Ag₂S、MnS、FeS₂)和氧化锰矿(主要含MnO₂)为原料联合提取银和锰的一种流程示意图如下。

(1)“浸银”时,使用过量FeCl₃、HCl和CaCl₂的混合液作为浸出剂,将Ag₂S中的银以[AgCl₂]⁻形式浸出。
将“浸银”反应的离子方程式补充完整:2Fe³⁺+ Ag₂S+ 4Cl⁻ ⇌ 2Fe²⁺ + 2[AgCl₂]⁻ +S
(2)“沉银”过程中需要过量的铁粉作为还原剂。该步反应的离子方程式有2[AgCl₂]⁻ +Fe =2Ag +Fe²⁺ +4Cl⁻;Fe +2Fe³⁺ =3Fe²⁺
2️⃣2023·新课标卷
铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以Cr₂O₇²⁻存在,在碱性介质中以CrO₄²⁻存在。
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为Na₂CrO₄。
(2)“还原”步骤中加入焦亚硫酸钠(Na₂S₂O₅)溶液,反应的离子方程式为2Cr₂O₇²⁻ +3S₂O₅²⁻ +10H⁺ =4Cr³⁺ +6SO₄²⁻ +5H₂O。
3️⃣2023·辽宁卷
某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni²⁺、Co²⁺、Fe²⁺、Fe³⁺、Mg²⁺和Mn²⁺)。
实现镍、钴、镁元素的回收。
(1)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸H₂SO₅ ,1mol H₂SO₅中过氧键的数目为NA.
- 1*a+2*(5-a)=8;a=2
- H—O—O—H
(2)“氧化”中,用石灰乳调节pH=4,Mn²⁺被H₂SO₅氧化为MnO₂,该反应的离子方程式为Mn²⁺ +HSO₅⁻ +H₂O =MnO₂ +SO₄²⁻ +3H⁺(H₂SO₅的电离第一步完全,第二步微弱);滤渣的成分为MnO₂、Fe(OH)₃。
- H₂SO₅可以把Fe²⁺氧化成Fe³⁺
- Fe³⁺在pH=3.1时开始沉淀
(3)“沉钴镍”中得到的 Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为4Co(OH)₂ +O₂ =4CoO(OH) +2H₂O
4️⃣2023·宁夏银川一中校考三模
HDS 催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧 ——水浸取法从 HDS 废催化剂(主要成分为MoS、NiS、V₂O₅、Al₂O₃)中提取贵重金属钒和钼,其工艺流程如图所示。
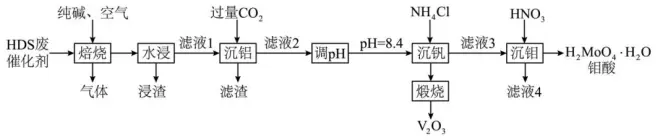
已知:MoO₃、V₂O₅、Al₂O₃均可与纯碱反应生成对应的钠盐,而NiO不行。
- 对应的钠盐是不发生化合价变化的
(1)“浸渣”的成分为NiO;“滤液 2”中的成分除了Na₂MoO₄外,还含有NaHCO₃、NaVO₃。
- 注意:AlO₂⁻ +CO₂ +2H₂O =Al(OH)₃ +HCO₃⁻
(2)请写出“焙烧”过程中MoS与纯碱反应的化学方程式:2MoS +2Na₂CO₃ +5O₂ =焙烧= 2Na₂MoO₄ +2SO₂ +2CO₂
- 高温焙烧下,Na₂CO₃和O₂会变成CO₂
5️⃣2023·辽宁省六校高三上学期期初考试
硼氢化钠(NaBH₄)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃)。工业上可用硼镁矿(主要成分为 Mg₂B₂O₅·H₂O,含少量杂质Fe₃O₄)制取 NaBH₄,其工艺流程如下:

高温合成发生的化学方程式为Na₂B₄O₇ +7SiO₂ +8H₂ +16Na =高温= NaBH₄ +7Na₂SiO₃
- H₂:Na =1:2
- Na₂B₄O₇好固定

