从暗影中伸出的魔爪——索戈托病毒

今天介绍的是最危险的正黏病毒——索戈托病毒(托高土病毒,Thogotovirus)。

索戈托病毒(托高土病毒,Thogotovirus)是拥有包膜的RNA病毒,是正粘病毒科的七个属之一。它们的反义RNA基因组有6~7个片段。索戈托病毒与其他大多数正粘病毒的区别在于它们是虫媒病毒,即靠节肢动物传播的病毒,在这种情况下宿主通常是蜱虫。索戈托病毒可以在蜱虫细胞和脊椎动物细胞中复制;此外,还从蚊子中分离出一种亚型。索戈托病毒通过吸血节肢动物传播,在脊椎动物宿主中系统性传播——与流感病毒不同,流感病毒通过呼吸道飞沫传播,通常局限于呼吸系统。
索戈托病毒(托高土病毒,Thogoto Virus,Thogoto Thogotovirus、THOV)是索戈托病毒代表毒株。除此以外,它还包含德里病毒(Dhori Virus、Dhori Thogotovirus、DHOV)及其亚种巴特肯病毒(Batken Virus、Batken Thogotovirus、BATV),以及阿拉瓜里病毒(Araguari Virus、Araguari Thogotovirus、ARAV),阿兰萨斯湾病毒(Aransas Bay Virus、Aransas Bay Thogotovirus、ABV),波本病毒(Bourbon Virus、Bourbon Thogotovirus、BRBV),乔斯病毒(Jos Virus、Jos Thogotovirus、JOSV)、乌普鲁病毒(Upolu Virus、Upolu Thogotivirus、UPOV)和奥兹病毒(Oz Virus、Oz Thogotovirus)。索戈托病毒主要感染哺乳动物,有时也会感染鸟类,主要引起牲畜疾病。索戈托病毒、德里病毒和波本病毒可以感染人类,并偶尔与人类疾病有关。
病毒历史
1960年代初分别在肯尼亚和印度发现了索戈托病毒和德里病毒。1966年发生了2例与索戈托病毒相关的人类疾病病例,1980年代的一次俄罗斯实验室事故表明德里病毒也可以引起人类疾病。这两种病毒最初被认为是布尼亚病毒,但在1980年代和1990年代初期的特征表明它们与流感病毒相似。1995年提出了正粘病毒科中的一种“索戈托病毒”,并于次年被ICTV命名为“索戈托病毒”。这个名字来自肯尼亚的索戈托森林,是索戈托病毒第一个被发现的地方。此后,对5种在1960-70年代发现但未分类或暂定属于布尼亚病毒的序列分析导致它们被提议作为该属的其他成员。该属的另一提议成员于2014年进行了下一代测序。
病毒的特征
索戈托病毒通常是球形或卵形,外部有包膜,直径在80-120 nm之间。在索戈托病毒、巴特肯病毒和波本病毒中观察到一些丝状形式。
索戈托病毒的反义RNA基因组是线性且分段的,具有六个或七个0.9-2.3 kb的片段,总大小约为10 kb。在蜱和感染了一种以上索戈托病毒的哺乳动物中都观察到了菌株之间片段的重排,但其在自然感染中的重要性尚不清楚。
病毒蛋白质
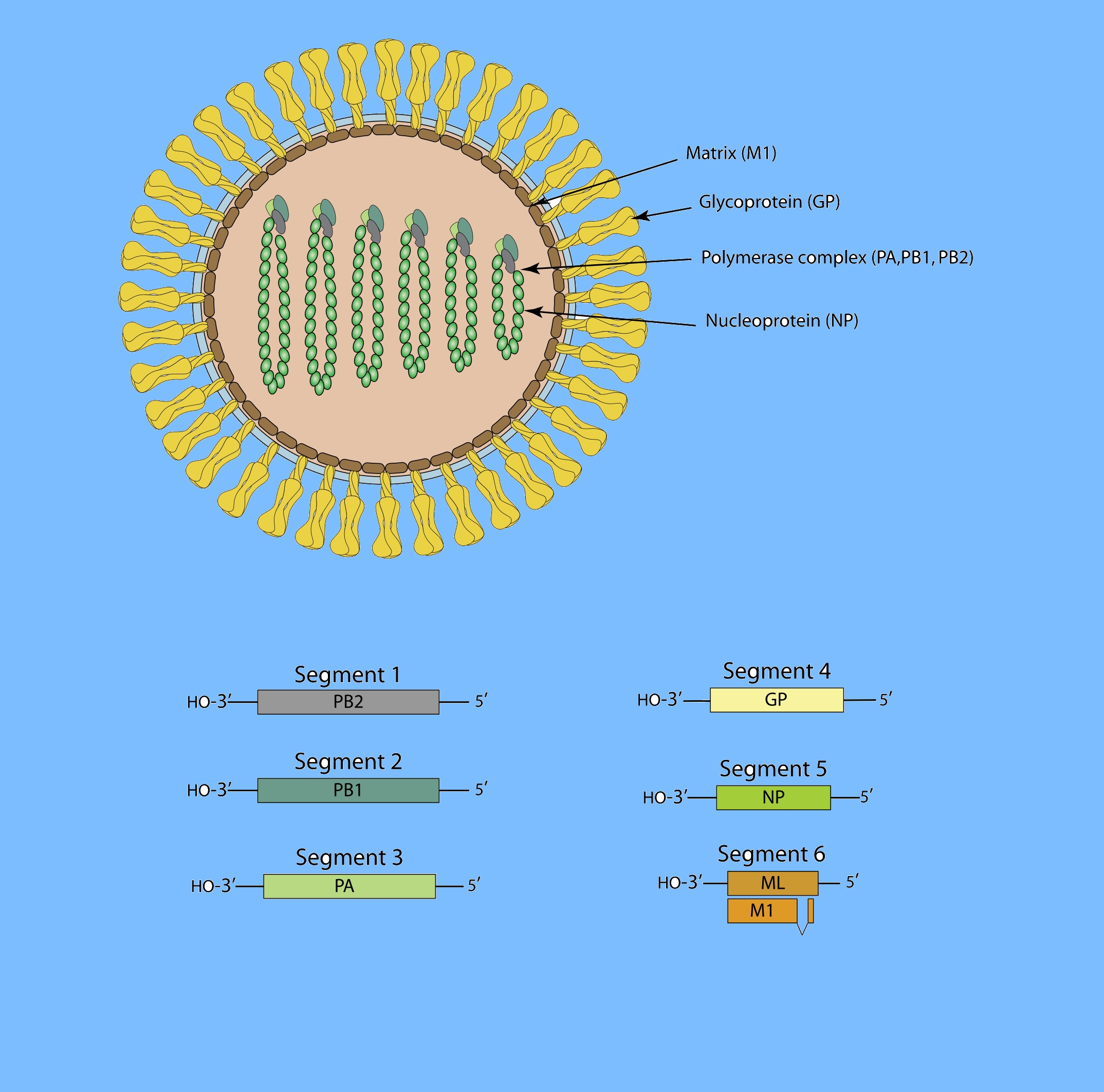
基因组编码7–9种蛋白质,包括三聚体RNA聚合酶(PA、PB1、PB2)和与病毒基因组结合的结构蛋白核蛋白(NP);基质蛋白(M1)和棘突蛋白(GP)分布在病毒的包膜之上。

索戈托病毒棘突蛋白与流感病毒糖蛋白(血凝素和神经氨酸酶)完全不同,而是与杆状病毒的GP64糖蛋白相似,后者感染昆虫。它也与夸兰菲尔病毒(Quaranfil quaranjavirus)的血凝素相似,夸兰菲尔病毒是蜱传正粘病毒的新属类型。
索戈托病毒获得杆状病毒样糖蛋白的机制尚不清楚。Pat Nuttall及其同事推测,此次蛋白俘获使这些病毒能够感染蜱。这种对节肢动物细胞的明显受体特异性并不能阻止大多数索戈托病毒感染脊椎动物。索戈托病毒糖蛋白被分类为III类抗原,缺少流感病毒血凝素(I类抗原)中存在的融合肽。
索戈托病毒和乔斯病毒还编码M-Long(M-L)蛋白,该蛋白对抗宿主的先天免疫力,特别是通过抑制干扰素的产生。 这种逃避免疫对于病毒在脊椎动物中的全身感染很重要,但在节肢动物中则是不必要的,因为节肢动物缺乏干扰素的应答。M-L的作用机制与流感病毒(NS1)中的等效蛋白质完全不同。
与所有正粘病毒一样,最大的三个区段(1-3)编码RNA聚合酶的三个亚基。 在索戈托病毒中,区段4编码糖蛋白,区段5编码核蛋白。 片段6的信使RNA(mRNA)可以剪接编码基质蛋白,也可以不剪接编码M-L,M-L在其C末端还有38个氨基酸。德里病毒中尚未发现第七部分的产物。
生活史
索戈托病毒的棘突蛋白通过与脊椎动物宿主细胞上的唾液酸结合诱导内吞,从而进入细胞。一旦囊泡被酸化,病毒和细胞膜就会发生融合。与其他正黏病毒一样,病毒的转录和复制都发生在细胞核中。在该属的某些成员中,复制已显示对Mx1/MxA蛋白敏感,Mx1/MxA蛋白是在小鼠和人类中对干扰素的反应诱导的。一项研究表明,这种抑制作用是由于MxA阻止了索戈托病毒基因组向核内的转运。
由于正粘病毒不编码加帽酶,因此转录的起始涉及病毒切下宿主mRNA的5'端的帽,因此该mRNA可被宿主翻译机制识别。 其他正粘病毒也使用类似的“抓帽”方法,但更长的宿主RNA序列会与帽一起切割并整合到病毒mRNA中。
病毒在细胞膜上组装,并通过出芽离开细胞。对于在小仓鼠肾细胞中生长的索戈托病毒,病毒颗粒在感染后6-8小时开始释放,在感染24小时后仍大量产生。 该增长速度比流感病毒慢,并且与夸兰费尔病毒更相似。
流行病学研究
已证明大多数索戈托病毒可感染节肢动物,通常是硬蜱或软蜱,它们是蛛形纲动物,但传染源蚊子是昆虫。索戈托病毒还感染鸟类和各种各样的野生和家养哺乳动物,包括有袋动物,啮齿动物,野兔,猫鼬,马,骆驼,山羊, 绵羊和牛。已经显示出三种类型的病毒——索戈托病毒、德里病毒和波本病毒感染人类。它们具有广泛的地理范围。
引发的疾病
在实验室环境中,该属的几个成员在小鼠和仓鼠中引起严重疾病。病毒会发生全身性传播,并在包括大脑、肝脏、淋巴系统在内的多个器官和系统,有时甚至在肺和小肠中引起病理作用,淋巴细胞是德里病毒的主要靶细胞。小鼠的德里病毒感染类似于小鼠和雪貂的实验性流感病毒感染,以及人类的致命H5N1流感病毒感染,并已被提议作为这种疾病的模型。
在哺乳动物中,索戈托病毒自然感染通常不会引起症状。
波本病毒于2014年首次发现于堪萨斯州东部波本县,密苏里州也有发生。患者有发烧,发冷,虚弱,厌食,头痛,肌痛,关节痛,恶心和腹泻等“感冒”样症状,有蜱虫咬史。胸、腹和背弥漫性黄斑丘疹和非痛性左腋窝腺病。白细胞减少,血小板减少和天冬氨酸转氨酶水平升高。患者被认为是蜱传疾病,接受强力霉素治疗,但肺,肝和肾功能恶化,在发病后11天死亡。蜱传病原体和美国疾病控制与预防中心检测的既往病毒均阴性。电子显微镜发现病毒颗粒,核酸测序和系统发育分析揭示凶手为波本病毒。
治疗方式
截至2015年2月,尚无针对索戈托病毒的特异性治疗方法或疫苗。抗病毒药物利巴韦林具有广泛的活性,其中包括一些其他正粘病毒,在一项研究中已显示其可在体外抑制德里病毒复制。支持疗法用于索戈托病毒疾病,并已被美国疾病控制与预防中心推荐用于波本病毒的感染。 与其他虫媒病毒一样,避免与传染动物接触是预防的关键。

