7种细胞死亡全整合,基于RCD进行肿瘤分型+多组学分析+预后模型+实验验证,一把拿下8分

2023年了,还是想在细胞死亡方向深耕一下,看看有没有潜在的细胞死亡新热点、新思路能发高质量生信文章?

一般有三条路:一个是刚爆出来的热点抢发纯生信,比如前两天提出的“双硫死亡”和去年爆火的“铜死亡”,这条路要想发高分就是需要眼疾手快赶上热点红利期
另一条路就是在思路上创新,热点串联可以做“多个细胞死亡形式的整合分析”或者“细胞死亡联合其他热点(m6A、氧化应激、线粒体等)分析”··· 还可以在分析内容上增加些亮点,比如多组学分析(转录组+基因组+表观组)···
最后一条路就是加验证实验,走干湿结合的路子,这也是生信发展的大趋势,并且这个趋势已经到来了~ ~

小云这次分享一篇8分+ 细胞死亡方向思路创新+验证实验,两条路联合的文章——基于7种调节性细胞死亡(RCD)进行肿瘤分型分析+多组学分析+预后模型构建+实验验证,干湿结合大趋势下妥妥的8分+质量!附带7种RCD基因集合,换个疾病就能复现啦,心动不如行动哦

l 题目:关于非小细胞肺癌预后和免疫景观的特异性调节细胞死亡相关分型
l 杂志:Front. Immunol.
l 影响因子:IF=8.786
l 发表时间:2023年2月
数据来源

研究流程
基于TCGA数据库中3429个RCD相关基因进行一致性聚类,确定了5个非小细胞肺癌亚组,并描述了这些亚组的基因组特征、免疫景观和免疫治疗/化疗反应的特征。筛选正常和肿瘤样品之间的差异RCD相关基因,单变量cox回归分析筛选与OS显著相关的基因,Lasso回归和多变量Cox回归构建基于53个RCD相关基因的预后模型,并进行模型评估和验证。分析RCD风险模型对免疫疗法和化疗反应的预测作用,分析关键基因LDLRAD3表达与预后的相关性,并在细胞样本中验证其功能。
主要结果
1. 基于RCD相关基因的非小细胞肺癌分型分析
使用RCD相关基因的表达矩阵进行无监督聚类分析(ps:私信小云获得基因集合哦),获得了五种不同的NSCLC亚型(图1A)。KM生存曲线分析5种亚型间的预后差异(OS、DFI、PFI)(图1D-F)。GSVA分析5种亚型之间细胞死亡相关途径的富集分数差异(图1I)。(ps:KM生存曲线绘制、GSVA分析也可以用小云新开发的零代码生信分析小工具实现,云生信分析工具平台包含超多零代码分析和绘图小工具,上传数据一键出图,感兴趣的小伙伴欢迎来尝试哟,网址:http://www.biocloudservice.com/home.html)。
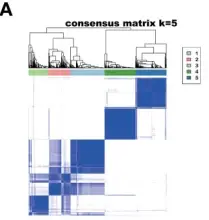






图1 基于RCD的分型分析
2. 不同聚类中肿瘤微环境与化疗反应分析
在TME中,三级淋巴结构(TLS)被认为是免疫细胞的生发中心,所以首先评估了5个亚型中一系列参与TLS形成的趋化因子的表达差异(图2A)。然后通过xCELL算法分析5个亚型中免疫细胞和基质细胞的比例(图2B),并进一步计算了5个亚型中的免疫得分、基质得分、估计得分(图2D)和免疫检查点基因的表达(图2F)。由于化疗是非小细胞肺癌治疗的基础,所以最后评估了每个亚型对化疗的反应(图2H)。(ps:在TME相关分析中分析TLS的比较少,比较新颖,分析又比较简单,这一点可以学起来哦!另外,TLS也可以单独作为一个方向来做生信分析,小云之前也分享过TLS生信思路,感兴趣的小伙伴可以公众号搜索观看)





3. 不同亚型间的富集途径、体细胞突变和DNA甲基化模式多组学分析
通过GSVA分析研究了5个亚型中的富集途径(图3A)。通过R package MAF tools评估了5个亚型中RCD相关基因的体细胞突变(图3B)和拷贝数变异(图3C),通过R package ChAMP评估了RCD相关基因的差异甲基化位点(图3E)。




图3 多组学分析
4. RCD风险模型的建立与验证
筛选正常和肿瘤样品之间的差异RCD相关基因,单变量cox回归分析筛选与OS显著相关的基因,通过LASSO/Cox回归建立基于53个RCD基因的风险模型(图4A)。根据风险评分中位数分为高风险组和低风险组,进行KM生存分析并利用ROC曲线评估模型的敏感性和特异性(图4C, D),在GEO验证集中进行模型验证(图4E, F)。利用Cox回归模型评估RCD风险评分的独立预后价值(图4J)。(ps:单因素/多因素Cox回归、LASSO回归分析都可以用小云新开发的零代码生信分析小工具实现哦,感兴趣的小伙伴欢迎来尝试,网址:http://www.biocloudservice.com/home.html)。




图4 RCD风险模型的建立与验证
5. RCD风险模型对免疫疗法反应预测
首先利用KM曲线评估接受抗PD-1/PD-L1治疗的高和低RCD风险组NSCLC患者的PFS预后(图5A,B)。随后分析了IMvigor210队列中风险评分与免疫治疗反应的相关性(图5C, D),进一步使用肿瘤免疫功能障碍和排除(TIDE)评分来验证RCD-风险模型在预测免疫反应的优越性(图5E)。通过xCELL算法分析高和低RCD风险组中免疫细胞和基质细胞的比例(图5F),并进一步比较了两组间免疫检查点基因的表达(图5G)和TLS趋化因子的表达(图5K)。






6. 关键RCD预后基因的筛选和验证
为了验证RCD-Risk模型的临床可应用性,进一步分析了模型中的RCD基因,发现LDLRAD3 mRNA在癌症中的作用鲜有报道,所以后续将探索LDLRAD3的功能。首先KM生存曲线评估高或低LDLRAD3表达的NSCLC患者OS预后(图6A),单变量和多变量Cox分析确定了LDLRAD3的独立预后价值(图6B, C)。利用NSCLC标本的组织微阵列(RLN121e)验证LDLRAD3的表达,以及与预后的关系(图6D, E)。随后在NSCLC细胞中将LDLRAD3过表达,通过CCK8、克隆形成、transwell实验评估LDLRAD3对肿瘤增殖、迁移和侵袭能力的影响(图7)。






文章小结
这篇文章的分析内容比较丰富,数据量较大,先进行肿瘤分型和多组学分析,再构建风险模型,最后再加上关键基因的表达和功能验证,干湿结合打造出了1篇名副其实的8分+文章。目前这种将多种细胞死亡整合分析的生信文章还不多,也就是说让你去发挥的空间相当大哟,利用这篇文章搜集到的基因集合,换个癌种能复现,快行动起来吧!


