抗衰明星NR、NMN都是这个家族,顶级机构梅奥指明NAD+未来方向


近日,来自全球顶尖医疗机构梅奥诊所旗下医学院(Mayo Clinic College of Medicine)团队在Aging Cell上发表了一篇关于NAD+代谢与衰老的综述[1]。综述全面系统讲述团队对大热物质NAD+抗衰的独特看法,堪为领域后续研究指路明灯。
NAD+与衰老关系一直是研究热点,而自诞生以来就一直争议不断的抗衰明星补剂NR、NMN就是NAD+前体,派派一直帮大家追踪着这个领域的最新动态,自然也不会错过顶尖医疗机构这篇富有潜力的文章。


在说明NAD+在衰老领域为什么如此重要之前,我们先简单了解一下NAD+的合成和消耗,这是机体内NAD+水平变化的基础。
NAD+的合成主要有三种途径:以色氨酸(TRP)为起始的从头合成途径,以烟酸(NA)为起始的Preiss-Handler途径和有NR、NMN等抗衰明星物质参与的挽救途径。

图注:NAD+代谢途径。从左到右依次为:色氨酸(Trp)通过中性氨基酸蛋白质载体进入细胞参与从头途径;NA由膜载体进入细胞用于Preiss-Handler途径;NR和NMN分别通过特定的转运蛋白进入细胞,参与挽救途径
在目前的研究中发现,NAD+的消耗主要与CD38、PARP、Sirtuins和SARM1这几种NAD+消耗酶有关。
其中CD38是哺乳动物最主要的NAD+消耗酶;PARP酶和长寿蛋白Sirtuins以NAD+作为底物参与DNA损伤修复、细胞增殖、衰老、凋亡等多个生物学过程;SARM1则是神经系统中重要的NAD+消耗酶。

作为机体氧还原反应中必不可少的辅酶和非氧化还原反应中的底物,大到心血管病、阿尔兹海默症等年龄相关疾病,小到细胞衰老,NAD+代谢水平的变化可谓是与衰老息息相关。
1. 衰老过程中NAD+水平降低
NAD+不可忽视的重要性,自然也引起了人们对生物体内NAD+水平的关注。研究者们发现,这种重要的辅酶在衰老过程中会发生代谢障碍,在体内含量逐渐减少。
根据过往的经验我们知道,物质的减少必然与其产生和消耗途径的变化有关,NAD+同样也不例外。总结众多研究结果后作者发现,在衰老过程中,NAD+的合成减少而消耗增多。

在NAD+合成的挽救途径中,NA、NMN等前体转化为NAD+需要NAMPT、NMNAT等酶的参与,而这些酶在体内的含量和活性都会随着衰老而下降,导致通过挽救途径合成的NAD+量减少。
另外,NAD+的从头合成途径中的QPRT酶也会在衰老过程中表达降低,导致从头合成途径失调,最终使NAD+合成减少。
消耗增加则与CD38、PARP等NAD+消耗酶活性在衰老过程中增加直接相关。
例如,研究人员发现作为NAD+分解酶(NADase)的CD38,其水平和活性在衰老过程中增加,敲除小鼠的CD38后,NAD+水平得到了保留。又如,DNA损伤水平随着年龄的增长而增加,负责DNA修复的酶PARP1活性增加,消耗了更多的NAD+。
另外,部分微生物在体内的代谢活动有助于增加体内的NAD+水平,比如细菌在烟酰胺酶PnCA介导下的脱酰胺作用能产生NA和NAR,有助促进口服补剂NAM和NR的NAD+增强作用。因此,衰老过程中的肠道生态失调可能损害这些微生物促进NAD+的作用。
2. 年龄相关疾病中总能看到NAD+代谢障碍的身影
与体内NAD+水平下降这一较微观的变化相比,年龄相关疾病总是更容易引起人们的担忧。
作者总结了心血管疾病、癌症、与年龄相关的代谢紊乱、器官纤维化、神经退行性疾病和短端粒综合征中NAD+水平的变化,发现NAD+水平下降就像影子一样,总是与衰老和年龄相关疾病同时出现。

3. NAD+水平与衰老经典标识“细胞衰老”关系密切
2013年顶刊Cell上刊登的“衰老9大标识”(在2023年新增至12个)为衰老研究确定了框架,本文作者重点阐述了衰老标识中的“细胞衰老”与NAD+代谢之间的关系。
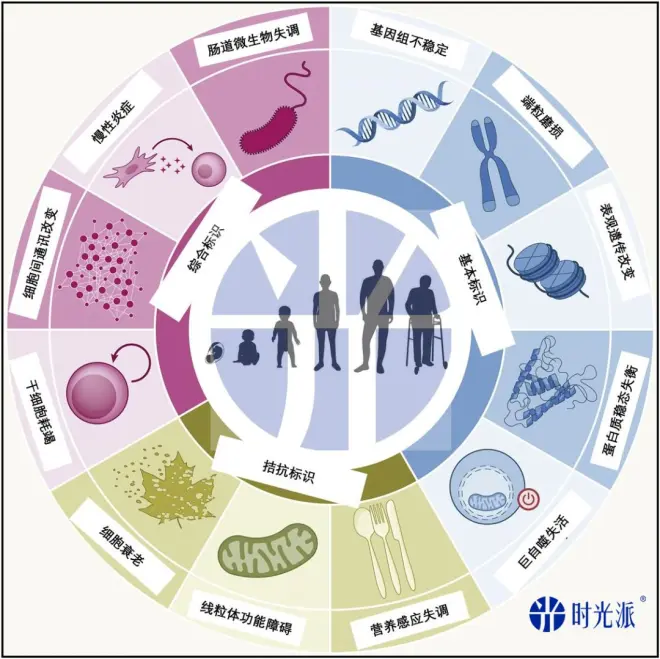
图注:衰老12大标识
低水平NAD+对细胞衰老进程来说就像一把双刃剑。一方面,低水平NAD+引起的DNA损伤和线粒体功能障碍会加速细胞衰老;另一方面,细胞衰老进程又需要较高水平的NAD+去维持,从这个角度来说,低水平NAD+又抑制了细胞衰老。
兴许衰老细胞践行的是“以彼之道,还施彼身”原则,低NAD+水平对细胞衰老进程有利有弊,衰老的细胞对NAD+水平的影响同样也有好有坏。
好处是,衰老细胞增加了NAMPT酶的释放,这是一种NAD+限速酶,它的增加可以促进NAD+的合成。但坏处是,这种酶同时也会诱导细胞产生促炎促衰的SASP。同时,衰老细胞会诱导和募集消耗NAD+的CD38细胞,导致NAD+水平下降。

图注:图注:细胞衰老与NAD+代谢的相互作用

因为NAD+代谢失调总是发生在衰老和各种年龄相关疾病中,所以有学者提出恢复NAD+水平可能是促进健康衰老的潜在方法。目前学界采用口服NR、NMN等前体补充NAD+,以研究提升NAD+水平是否有助于治疗年龄相关疾病。
在开展的各项临床前研究(也就是动物实验)中,提升NAD+水平表现出良好的抗衰作用,有治疗多种年龄相关疾病的潜力。
比如,在患有心血管疾病的小鼠中,采用口服NMN、CD38抑制剂和PARP抑制剂等方式增强NAD+水平之后,小鼠的心血管疾病得到了改善。
这几种提升NAD+水平的方式在治疗癌症、减少纤维化、缓解代谢失调和治疗神经退行性疾病方面也发挥了一定的积极作用。

虽然目前关于提升NAD+水平治疗年龄相关疾病的人体临床实验较少,尚不清楚特定疾病是否会从NAD+前体补充中受益。但是,现有的NR和NMN的临床试验已经证明了它们在短期给药中是安全的,并且能有效提升人体内的NAD+水平。
良好的临床前研究结果和目前表现为安全的NAD+前体临床研究,让学界对于NAD+抗衰的研究保持着乐观态度,未来的研究可能更多的倾向于探清NAD+增强措施会改善哪些衰老标识,以及在人体中能治疗哪些年龄相关疾病。
值得一提的是,作者非常看好将senolytic疗法(一种旨在清楚衰老细胞的经典抗衰疗法)与NAD+增强治疗相结合,认为这可能会提高NAD+靶向干预的安全性和有效性。
Senolytics可以选择性地杀死衰老细胞,减少整体的老年负担,而NAD+前体补充剂能提高细胞的NAD+水平,帮助细胞维持健康的能量代谢,二者的协同效应可能产生1+1 >2的抗衰效果。

图注:Senolytics和NAD+增强疗法联合使用以促进健康衰老的理论框架
Aging Cell的这篇综述不仅全面阐释了NAD+在衰老过程中的变化,而且客观评价了NAD+补充治疗对抗衰的作用。联系到前段时间NR无用的新闻,相信这篇文章一定能解答读者朋友们关于补充NAD+抗衰的一些疑问。
虽然目前补充NAD+抗衰的人体临床证据还有一定不足,但这不影响学界对这一大热抗衰疗法的信心。另外,乐观的派派相信,作者提出的Senolytics和NAD+补剂这两个经典抗衰方式的强强联合,未来一定能让抗衰领域的研究更加蓬勃。
最后插播一条消息,美国宾夕法尼亚大学教授Joseph Baur一直深耕NAD+临床研究,派派有幸邀请到这位教授莅临年底的衰老干预论坛。欢迎各位对NAD+感兴趣的朋友届时一起到现场与这位学术大咖交流互动,共同探寻NAD+抗衰延寿的秘密!
—— TIMEPIE ——

参考文献
[1] Chini CCS, Cordeiro HS, Tran NLK, Chini EN. NAD+ metabolism: Role in senescence regulation and aging [published online ahead of print, 2023 Jul 9]. Aging Cell. 2023;e13920. doi:10.1111/acel.13920
[2] Stock AJ, Ayyar S, Kashyap A, et al. Boosting NAD+ ameliorates hematopoietic impairment linked to short telomeres in vivo [published online ahead of print, 2023 Feb 24]. Geroscience. 2023;10.1007/s11357-023-00752-2. doi:10.1007/s11357-023-00752-2
[3] Hou Y, Wei Y, Lautrup S, et al. NAD+ supplementation reduces neuroinflammation and cell senescence in a transgenic mouse model of Alzheimer's disease via cGAS-STING. Proc Natl Acad Sci U S A. 2021;118(37):e2011226118. doi:10.1073/pnas.2011226118
[4] Yang B, Dan X, Hou Y, et al. NAD+ supplementation prevents STING-induced senescence in ataxia telangiectasia by improving mitophagy. Aging Cell. 2021;20(4):e13329. doi:10.1111/acel.13329
[5] Morevati M, Egstrand S, Nordholm A, et al. Effect of NAD+ boosting on kidney ischemia-reperfusion injury. PLoS One. 2021;16(6):e0252554. Published 2021 Jun 1. doi:10.1371/journal.pone.0252554
[6] Doke T, Mukherjee S, Mukhi D, et al. NAD+ precursor supplementation prevents mtRNA/RIG-I-dependent inflammation during kidney injury. Nat Metab. 2023;5(3):414-430. doi:10.1038/s42255-023-00761-7
[7] Mills KF, Yoshida S, Stein LR, et al. Long-Term Administration of Nicotinamide Mononucleotide Mitigates Age-Associated Physiological Decline in Mice. Cell Metab. 2016;24(6):795-806. doi:10.1016/j.cmet.2016.09.013
[8] Aflatounian A, Paris VR, Richani D, et al. Declining muscle NAD+ in a hyperandrogenism PCOS mouse model: Possible role in metabolic dysregulation. Mol Metab. 2022;65:101583. doi:10.1016/j.molmet.2022.101583
[9] Margier M, Kuehnemann C, Hulo N, et al. Nicotinamide Mononucleotide Administration Prevents Doxorubicin-Induced Cardiotoxicity and Loss in Physical Activity in Mice. Cells. 2022;12(1):108. Published 2022 Dec 27. doi:10.3390/cells12010108
[10] Yoo KH, Tang JJ, Rashid MA, et al. Nicotinamide Mononucleotide Prevents Cisplatin-Induced Cognitive Impairments. Cancer Res. 2021;81(13):3727-3737. doi:10.1158/0008-5472.CAN-20-3290
[11] Zhang Y, Zhu W, Wang M, Xi P, Wang H, Tian D. Nicotinamide mononucleotide alters body composition and ameliorates metabolic disorders induced by a high-fat diet. IUBMB Life. 2023;75(6):548-562. doi:10.1002/iub.2707
[12] Mitchell SJ, Bernier M, Aon MA, et al. Nicotinamide Improves Aspects of Healthspan, but Not Lifespan, in Mice. Cell Metab. 2018;27(3):667-676.e4. doi:10.1016/j.cmet.2018.02.001
[13] Hu S, Wang S. The Role of SIRT3 in the Osteoporosis. Front Endocrinol (Lausanne). 2022;13:893678. Published 2022 May 25. doi:10.3389/fendo.2022.893678
[14] Roboon J, Hattori T, Ishii H, et al. Inhibition of CD38 and supplementation of nicotinamide riboside ameliorate lipopolysaccharide-induced microglial and astrocytic neuroinflammation by increasing NAD+. J Neurochem. 2021;158(2):311-327. doi:10.1111/jnc.15367
[15] Escande C, Nin V, Price NL, et al. Flavonoid apigenin is an inhibitor of the NAD+ ase CD38: implications for cellular NAD+ metabolism, protein acetylation, and treatment of metabolic syndrome. Diabetes. 2013;62(4):1084-1093. doi:10.2337/db12-1139
[16] Langley MR, Choi CI, Peclat TR, et al. Critical Role of Astrocyte NAD+ Glycohydrolase in Myelin Injury and Regeneration. J Neurosci. 2021;41(41):8644-8667. doi:10.1523/JNEUROSCI.2264-20.2021
[17] Peclat TR, Thompson KL, Warner GM, et al. CD38 inhibitor 78c increases mice lifespan and healthspan in a model of chronological aging. Aging Cell. 2022;21(4):e13589. doi:10.1111/acel.13589
[18] Tarragó MG, Chini CCS, Kanamori KS, et al. A Potent and Specific CD38 Inhibitor Ameliorates Age-Related Metabolic Dysfunction by Reversing Tissue NAD+ Decline. Cell Metab. 2018;27(5):1081-1095.e10. doi:10.1016/j.cmet.2018.03.016

