萌新开坑w——小评(−)-Glaucocalyxin A首次全合成
前言
笔者大一小菜鸡一只😶,努力学有机ing~
考试周复习晕了,不务正业一把,之前北大贾彦兴教授课题组发了一篇有意思的Angew,点开一看是个四环二萜,正巧这学期看了不少贝壳杉烷二萜骨架的合成,贾老师组这篇着实震得我不轻,趁不想学习的时候赶快发出来,作为自己第一篇灌水小文w~~
废话不多说,先看看这分子的相貌👀

毫无疑问,面对这一化合物,从哪个环开始切断决定了路线的思考方向。这类骨架的合成路线多是从蓝色标出的双环【3.2.1】辛烷骨架开始切断,第一刀往往作用在五元环那儿,作为官能化的收尾。而贾老师选择了一种与前人完全不同的切断策略,在合成的前期就构筑出双环【3.2.1】辛烷的结构。
下面来看看贾老师课题组做的逆合成分析:

逆合成分析:
首先对五元D环进行官能团转化,希望在最后实现羰基的引入,随后好戏开始: 首先从A环切断,走IMDA切断,然后进行Aldol切断得到具有双环【3.2.1】辛烷结构的化合物(11),而化合物11则是三价锰介导的自由基关环反应的结果。关环前体(12)又可以由简单的化合物合成出来……
从逆合成分析我们可以看出,此路线关键的两步在于中期自由基5—exo—dig关环反应的实现与后期IMDA引入A环。
合成路线小析
关环前体的构筑:

作者从简单的环己烯酮出发,加入格式试剂与 CuI原位转金属化发生1,4加成后与氰基乙酸乙酯反应得到(16),随后1,3二羰的α烷基化后水解脱硅,得到了关环前体(12)。
关环反应的实现:

下一步就是最核心的5—exo—dig的串联关环反应,作者一通优化选出的条件可以达到60%的收率。利用羰基阿尔法位容易产生自由基的特性,得到了化合物(8)。
IMDA前体的构筑

随后化合物 11 在二氯甲烷中用三氟乙酸处理脱去硅基得到化合物 18,室温 下收率 73%。而非水溶剂的体系成功保护了酯基未被水解。

化合物(18)在经典的硼氢化钠甲醇体系中还原成立体专一的醇,手性的来源是底物的endo面位阻。随后羟基在三乙胺做缚酸剂的条件下上硅基保护,酯接着被DIBAL-H彻底还原后用DMP氧化得到Aldol前体20的醛。

接下来,化合物20与烷基化的α-β不饱和酯,在2,6-DPP作大位阻Lewis酸的条件下发生一个插烯的不对称Aldol缩合。作者巧妙地利用大位阻Lewis酸的底物诱导手性控制,将Michael受体的γ位成功地连接到了醛基上面。

作者在文章中也给出了自己对于这一反应立体选择性的解释,其中过渡态2的大位阻Lewis酸与甲基的排斥,使得TS-2的能量过高,故在TS-1中是更优势的反应构象。

随后化合物21上MOM保护羟基,然后用酰胺交换下酯,得到了Weinreb酰胺22,22用其Weinreb酰胺的特性,与甲基格式试剂得到了单一取代的酮,后处理后以惊人的99%的收率分离出酮,随后三乙胺条件下做烯醇硅醚得到Denishefsky最喜欢用的diene( ),自此,另一核心步骤IMDA的反应前体骨架已经构筑完毕。
IMDA的实现

化合物10在二甲苯溶剂中,200摄氏度条件下,质子海绵存在下发生一步高产率的分子内Dies-Alder反应,立体选择性得到了非常好的控制。这一步反应对于整个全合成也是意义重大的,因为这一步骤成功实现了A环的构建,也同时将B环的开口闭合,非常巧妙,出神入化。
骨架的结构修饰
DA产物脱硅醚,原位发生甲基化。至此,目标产物的基本骨架已经构筑出来了。令人惊喜的是,从化合物11开始到21结束,化合物11的环外双键始终被保护的很好,作者选用了适宜的酸碱条件,使得不太稳定的环外双键结构得到了很好的保留而没有发生加成或者移位。作者非常富有先见之明地提前构筑了环外双键,而没有选择在第一步切断时使用官能团转化,足见作者合成功底的扎实。

这一步的选择性非常有趣,一般来说环己酮的选择性还原在大位阻负氢还原剂的条件下以a键产物为主,只有在小位阻还原条件下才会得到由扭转张力控制的e键产物。

这一步的选择性,笔者推测是因为从“a”面(强行)进攻的位阻,受BCD环的影响反而位阻更大了。而这一步作者放任了手性的错误,再后期还原得到了正确的构型,后面笔者还会介绍。

这一步脱硅基后氧化,这一步的目的是为下一步调构型做准备,作者设计的这一步在许多经典的合成路线当中都有体现,氧化调构型是一种非常经典的用于调整醇的构型的方式,如在化合物Upai-A的合成中有如下反应:

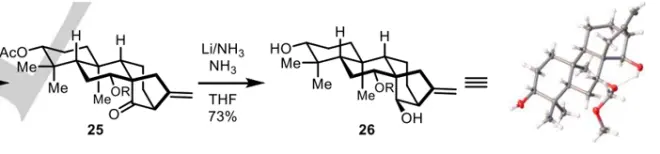
随后在锂/液氨的还原体系下,乙酰基被同步脱除掉了,以73%的产率一步构筑了带有正确手性醇构型的化合物26。
接下来用SeO2处理26选择性氧化到环外双键的α位,手性来源于底物的立体化学控制。

最后氧化后脱MOM保护,得到最终的目标产物。

总结:
我tm吹爆!!!
贾老师课题组在处理这一高氧化态的萜类分子时,考虑到羰基与羟基的天然转化关系,运用扎实的有机合成功底,将几个含氧基团逐步巧妙地构筑了出来,可谓非常出神入化,有条不紊。选择从AB环开始切断也是贝壳杉二萜化合物切断的一种新思路,切断的同时兼顾几个含氧基团的引入与氧化态转化,选用商业可得的简单含氧底物来实现目标化合物含氧基团的引入,整个路线简洁而精巧,让人看起来十分舒适。

参考文献:
Angew. Chem. Int. Ed. 10.1002/anie.202005932
后记()
一口气写完了w,第一次写这样的小文,心情十分的激动!!!在惊叹于别人超牛逼工作的同时,看着自己惨不忍睹的纸上合成,不由得感叹:“有机的天不是一般的高啊啊啊啊啊啊”
如果真的有人看的话。。。就准备加更第二期哈哈哈哈哈,不过眼下还是得先考完试......(爬走),也欢迎各位大佬激情怒对,我会很开心地接受大家的批评指正的!

