Trends Neurosci:大脑和行为性别差异的表观遗传学机制
大脑区域、行为和脑部疾病之间存在性别差异。大脑的性别分化是在产前开始的,但由于性腺激素、性染色体和环境三个主要因素的相互作用,它会在一生中持续。这些因素被认为在一定程度上通过表观遗传学机制发挥作用,表观遗传学控制脑细胞中的染色质和转录状态。
近日,美国福特汉姆大学生物科学系Marija Kundakovic和Maria Tickerhoof在Trends in Neurosciences上发表重要综述。在这篇综述中,作者讨论了表观遗传学机制在关键发育时期、整个发情周期以及不同环境的反应中导致性别特异性神经行为变化的证据。并进一步确定了该领域的未来方向,将为大脑性别差异提供新的机制见解,为脑疾病治疗,特别是女性的大脑健康提供信息。

1. 大脑的性别特异性特征:性腺激素、性染色体和环境的相互作用
啮齿类动物和人类在基因调控、神经化学、大脑结构、行为、大脑疾病以及对精神药物和其他环境因素的反应方面都存在性别差异。尽管人类大脑结构性别差异的影响大小和相关性一直存在争议,但据报道,不同疾病的大脑存在性别偏见,基于性别和性别的治疗可能会改变神经精神疾病。例如,抑郁症和焦虑症在女性中的患病率是男性的两倍,而自闭症谱系障碍在男孩中的发病率是女孩的四倍。在阿尔茨海默病、创伤后应激障碍(PTSD)、神经性厌食症、注意力缺陷多动障碍、多发性硬化症、帕金森病和精神分裂症等其他疾病中,症状的患病率和严重程度存在显著的性别差异。而表观遗传学机制是一个可能的候选者。
大脑的性别或性别特异性特征在一生中由三个主要因素的相互作用不断塑造:性腺激素、性染色体和环境影响[Fig.1]。在啮齿类动物和人类中,激素激增主要发生在生命的两个时期:围产期(雄性为睾酮)和青春期(雄性为睾丸激素,雌性为雌激素和黄体酮)。这些激素激增与大脑性别分化的两个重要时期相吻合。在青春期后,大脑受到激素作用的影响(这些激素在不同物种的雄性和雌性中具有激活作用)。在人类中,雌激素和黄体酮会发生周期性变化,直到女性进入更年期。人类更年期之前是更年期过渡或“围绝经期”,其特征是激素变化不规律。
压力、药物和饮食等环境暴露可能产生与性别无关的影响,也可能增加或减少大脑性别差异。性别通常分为女性、男性或双性人。人类的性别存在于一个范围内,包括(但不限于)女性、男性、非二元、性别和性别流动的个体。在顺性别个体中,性别认同与出生时指定性别相同的人。在变性人中,性别与出生时指定的性别不同。这些人可能会也可能不会选择通过性别确认程序,包括GAHT(性别确认激素疗法,会影响激素状态以及大脑的性别和性别相关特征)。
总之,对于每个个体来说,其性腺激素状态、性染色体补体和环境的独特相互作用将决定其大脑性别分化的状态。
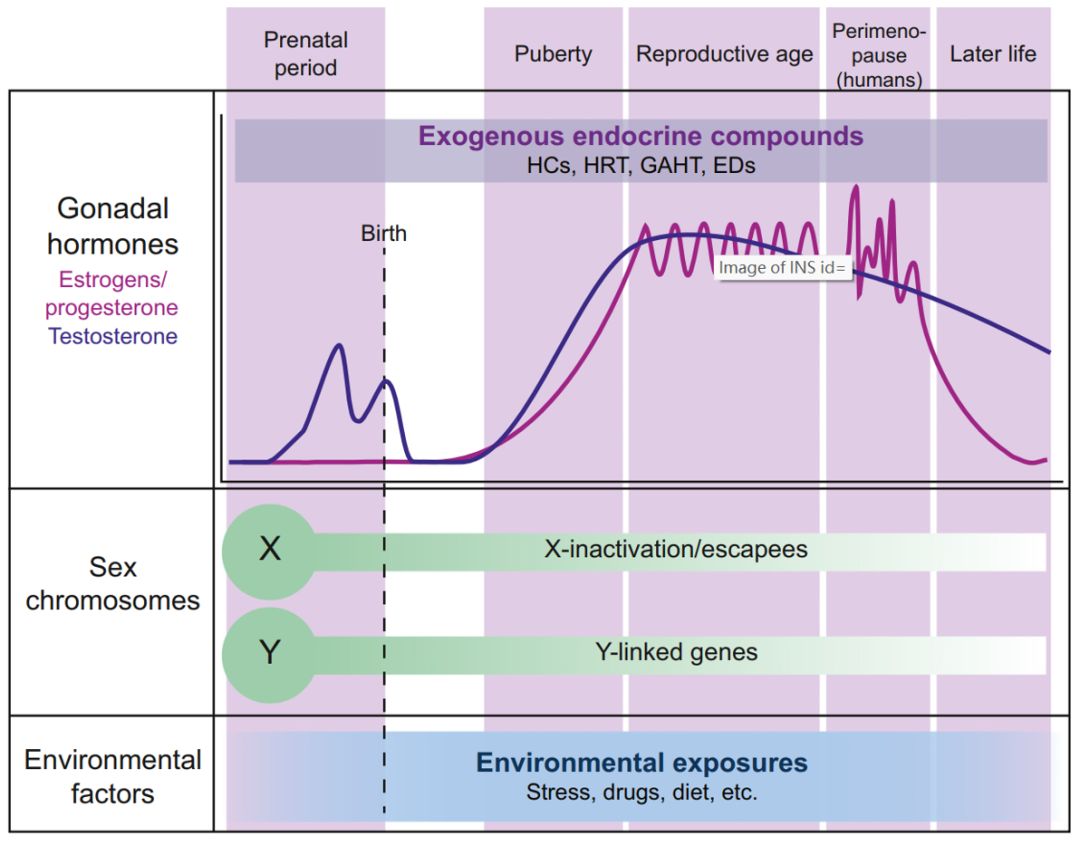
Figure 1 大脑的性别分化
2. 大脑表观遗传学调控
5基因表达的表观遗传调控的许多基本原理适用于神经科学。染色质是DNA和相关蛋白质(主要是组蛋白)的复杂结构,在表观遗传调控中发挥着核心作用[Fig.2]。DNA包裹在组蛋白周围,形成一种高度特殊的结构,称为染色质。最好的染色质修饰是DNA甲基化(Me)和组蛋白乙酰化和甲基化,所有这些都是动态的,可以直接或间接影响染色质的构型。胞嘧啶甲基化由DNA甲基转移酶(DNMT)催化,通常抑制基因转录。组蛋白乙酰化由组蛋白乙酰转移酶(HAT)“写入”,并由组蛋白脱乙酰酶(HDAC)“擦除”。组蛋白甲基化由残基特异性组蛋白甲基转移酶(HMT)“写入”,并由组蛋白去甲基化酶(HDM)“擦除”。
长非编码RNA(lncRNA)是另一种表观遗传学机制,可以募集染色质修饰蛋白并改变染色质构型。在染色质组织的第一个层次(1D染色质),人们可以看到核小体或“串上珠”型结构,其中147bp的DNA包裹在由H2A、H2B、H3和H4核心组蛋白组成的组蛋白八聚体上。其中一些组蛋白可以被影响染色质性质的组蛋白变体所取代。更高水平的染色质组织,也称为“3D基因组”,包括长程增强子-启动子相互作用、CTCF-loop和染色体区室,并与基因调控和神经元功能有关。通常,活性转录的基因位于细胞核内部的活性区室(常染色质),而非活性基因位于靠近细胞核纤层的非活性区室中(异染色质)。
总之,表观遗传学机制协同驱动染色质状态和基因表达,对大脑结构和功能的调节至关重要,包括在形成大脑性别差异方面。
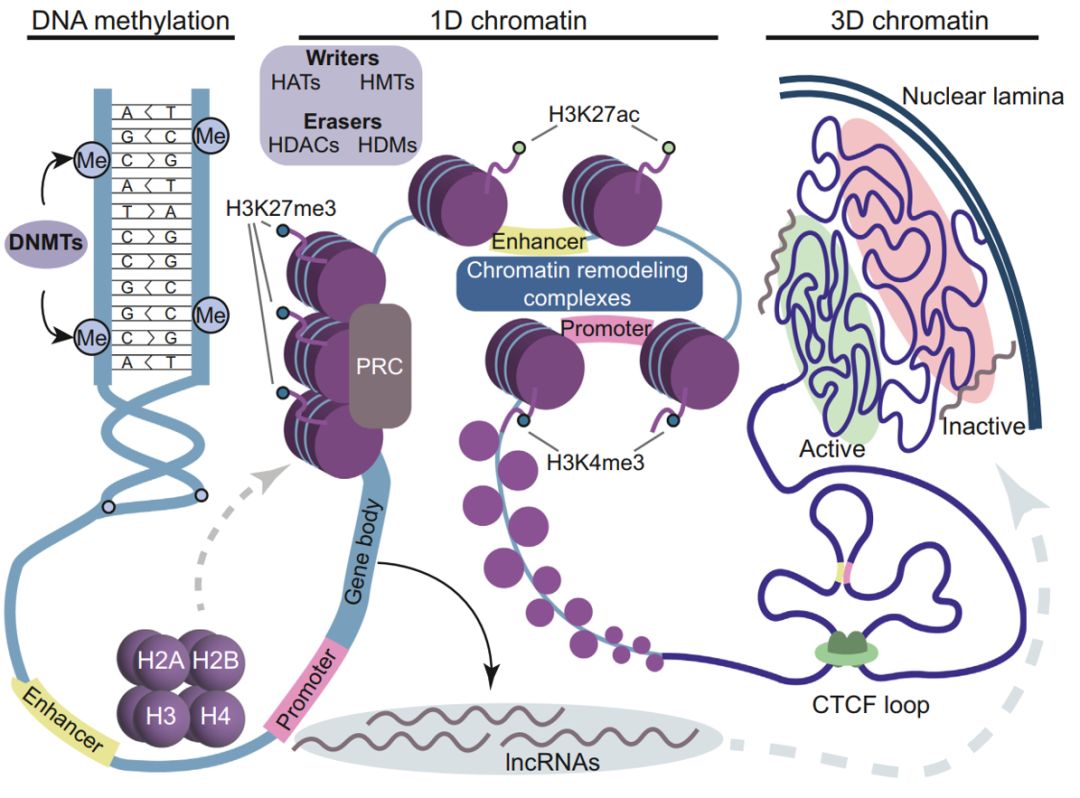
Figure 2 表观遗传学调控概述
3. 大脑中的性别特异性表观遗传学发现
3.1 性腺激素介导的表观遗传调控
雌性大鼠的雌二醇处理降低了DNMT活性并降低了POA中的DNA甲基化,而对新生鼠使用DNMT抑制剂(P0和P1期)处理模拟了雌二醇对雌性大鼠树突棘标记物的POA表达和性行为的影响,证实了DNA甲基化在大脑性别分化中的作用。虽然大脑的“女性化”被认为是一个更被动的过程,但最近的研究结果表明,大鼠大脑的女性化涉及到DNA甲基化对男性化基因的主动抑制,这为表观遗传学研究提供了新的证据。
3.2 性染色体相关的表观遗传学效应
X染色体失活是一个女性特有的过程,也是研究得最好的表观遗传学现象之一。然而,已知一些基因座(小鼠中约3-7%;人类中约15-25%)可以逃避X失活,尽管它们位于组成性抑制的环境中。这些基因缺乏失活基因特有的表观遗传学特征,并且远离抑制性基因组元件。有趣的是,一些核心逃亡者编码表观遗传学调节因子,如组蛋白去甲基化酶,从而为大脑中的性别特异性表观遗传学调控提供了明确的候选者。
3.3 环境对大脑表观基因组的影响
产前是表观基因组发生动态变化最显著的时期。早期的候选基因研究提供了一个概念证明,即环境诱导的胚胎/胎儿表观基因组的变化可能是对大脑和后期行为的性别特异性影响的基础。一个例子是怀孕期间的母亲压力与后代患神经精神疾病的风险增加有关,包括精神分裂症、抑郁症和自闭症。
环境因素也可以减少大脑中的性别差异,例如一些早期生活环境暴露。例如,在小鼠中,早期母体分离(P1-14)增强了雄性和雌性对可卡因诱导的条件性位置偏好(CPP)。此外,青春期对环境因素高度敏感,包括压力、营养状况等,所有这些都会影响HPG轴的功能,并对生殖功能产生影响。虽然所有这些因素都可能改变大脑表观遗传学,但有证据表明,营养状况会影响女性青春期的表观遗传学编程。成人压力暴露对大脑和行为也有显著影响,并与精神风险增加有关。早期研究证明了应激诱导的行为结果中的表观遗传学机制,但这些研究主要在雄性小鼠中进行。然而,到目前为止,很少有研究探讨成人压力对大脑表观基因组的性别特异性影响。
4. 表观遗传学机制驱动性别特异性神经行为表型的功能证据
新生雌性大鼠的雌二醇处理通过减少POA中的DNA甲基化而使大脑雄性化,而EED(PRC2成分)通过抑制ARC中的Kiss1启动子来抑制小鼠的青春期。这些表观遗传机制为大脑性别分化提供了功能证据。有假设提出,单个基因座的表观遗传学变化足以驱动性别特异性行为。例如,病毒介导的工程锌指蛋白递送靶向雄性和雌性小鼠海马中Cdk5启动子的组蛋白H3K9/14乙酰化。这导致雌性小鼠的恐惧记忆提取减弱,揭示了一种性别特异性表观遗传学机制。
总结
越来越多的证据表明表观遗传学机制在大脑和行为中形成性别差异的作用。具体而言,大脑性别差异的主要来源,包括性腺激素、性染色体和环境因素,都会影响大脑中的表观遗传调控,对性别特异性神经生物学和行为产生影响。
虽然性别的影响提供了重要信息,但在不知道基于性别变异性来源的情况下,很难确定所观察到的影响背后的上游调节因子和机制。通过检查性别特异性因素(如性腺激素状态)和环境因素之间的相互作用,预计未来的研究将揭示性别特异性受体机制、表观遗传学调节因子和驱动性别特异性神经行为表型的特定细胞群。
原文链接:
https://www.cell.com/trends/neurosciences/fulltext/S0166-2236(23)00225-4
参考文献
Kundakovic M, Tickerhoof M. Epigenetic mechanisms underlying sex differences in the brain and behavior. Trends Neurosci. 2023 Nov 13:S0166-2236(23)00225-4. doi: 10.1016/j.tins.2023.09.007. Epub ahead of print. PMID: 37968206.
编译作者:Young(brainnews创作团队)
校审:Simon(brainnews编辑部)


