机器学习识别Treg基因特征+预后+免疫治疗/药敏性预测,8分+Frontiers一把收入囊中

肿瘤相关生信现在竞争这么激烈,该怎么拿高分呢?
看看生信文章分布,基本就是预后(占比最高)、分型、转移和耐药,突破点又在哪里?
小云这回给朋友们展示个终极大招——将多个创新方向联合起来分析!就像乾隆皇帝喜欢的“各种釉彩大瓶”一样,要的就是花团锦簇的感觉,打眼一看就是拿高分的水平

小云说的这个“多个创新方向联合”可不是简单的多热点分析方向结合,而是不同层面都保证创新性。举个例子,疾病方向创新(选择肿瘤耐药/免疫治疗预测就比单纯做预后模型创新性高)+分析方向创新(选择T细胞,比如Treg/Th细胞、T细胞增殖/耗竭就比做干细胞创新性高)+分析方法创新(利用机器学习算法就比直接从GeneCards、MsigDB等数据库中获得某方向基因集合的创新性高)。

看懂了吗?下面就利用1篇8分+的“机器学习识别Treg基因特征+预后+免疫治疗/药敏性预测”文章来实践一下吧!
研究背景
前列腺癌被定义为“冷”肿瘤,具有免疫抑制微环境。Tregs普遍存在于几乎所有的癌症中,并且被认为代表了肿瘤诱导的免疫抑制的主要机制,因此,在癌症免疫疗法(CIT)领域迫切需要减少Tregs和控制Tregs功能以增加抗肿瘤免疫反应的策略。然而,Treg特异性mRNAs及其在评估Treg、预测预后与CIT反应中的应用尚未被研究。
数据来源

研究流程
基于从PBMC纯化的Treg和其他免疫细胞类型的42个转录数据集,提出了基于机器学习的计算框架,以识别Treg特异性mRNAs。与384个前列腺癌中差异表达的treg相关基因取交集后获得74个前列腺癌相关的Treg特异性mrna。利用单因素和多因素COX回归分析开发了基于5基因的Treg的预后特征(TILTregSig),随后进行生存分析、肿瘤免疫评分和免疫细胞浸润分析、GSEA分析、免疫治疗反应预测和化学药敏性分析等。

主要结果
亮点一:利用机器学习算法识别Treg特异性mRNAs,并构建前列腺癌RFS的预后模型(结果见流程图)
i. 使用R package“limma”进行Treg细胞和来源于PBMCs的其他免疫细胞之间的mRNAs的差异表达分析。共得到2407个在Treg细胞系中高表达而在其他免疫细胞系中下调的mRNA,被定义为Treg特异性mRNA;
ii. 为了获得前列腺癌相关的mRNAs,使用从3名健康供体和3名前列腺癌患者的PBMC挖掘的Tregs的基因表达谱(来源于Ngar-Yee Huen等人文章),鉴定得到384个差异表达基因。与上述2407个Treg特异性mRNA取交集,共得到74个前列腺癌相关的Treg特异性mRNA。
iii. 使用单变量Cox回归分析探索与RFS相关的TILTreg相关mRNA作为预后mRNA。基于多变量Cox回归模型和前向和后向变量选择程序,应用机器学习方法从用于监测前列腺癌预后的候选生物标志物中选择5个基因的最佳组合构建预后模型(TILTregSig)。(ps:因为前列腺癌疾病特殊性,初次治疗后复发和BCR的发病率很高,所以这里构建的是前列腺癌无复发生存率(RFS)预后模型)
亮点二:评估TILTregSig对前列腺癌中Tregs浸润的预测潜力
通常做风险评分与肿瘤免疫的关系会分析免疫浸润细胞、TME一些评分指标、免疫检查点基因表达等。这里在常规分析的基础上又着重分析了TILTregSig与Tregs浸润的关系,有点类似于实验中的正反验证,本身风险评分就是从Treg特异性基因中建立的,反过来再去利用它评估Treg浸润,正反论证风险评分的预测能力。
在常规免疫浸润分析发现TILTregSig和Tregs之间存在显著相关性之后,进一步分析TILTregSig与Tregs的标记基因(FoxP3和TGF-β1)的相关性(图1E)。随后,将TCGA数据集中的前列腺癌患者根据Treg浸润水平的中值分为Treg低组和高组,进行PCA分析和风险评分对比(图1G, H),并利用ROC曲线评估TILTregSig对Tregs浸润的预测能力(图1J)。

图1 TILTregSig可以作为前列腺癌Tregs浸润的预测因子
亮点三:评估TILTregSig对CIT反应和泛癌药物治疗抗性的预测潜力
文章用多个免疫治疗队列和GSCALite平台重点评估TILTregSig对CIT反应和泛癌药物治疗抗性的预测潜力,比单纯的预后模型+一点点简单药敏性分析的证据力强。


图2 TILTregSig对CIT反应和泛癌药物治疗抗性的预测潜力
加分点: TILTregSig 的基因表达和关键基因功能的实验验证
收集从3名健康供体和3名前列腺癌患者的外周血样本,从PBMCs中分离Tregs,并利用WB进行TILTregSig中5个基因的蛋白表达验证。对于关键基因RRM2,利用siRNA验证其干扰后对Tregs的抑制功能的影响。

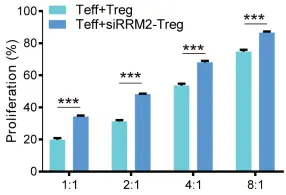
图3 TILTregSig 的基因表达和RRM2功能的实验验证
文章小结
本文既有疾病方向创新(肿瘤耐药/免疫治疗预测)+分析方向创新(Treg细胞)+分析方法创新(机器学习)的多层面创新叠加buff,又有湿实验的加持,数据量相当充实,可谓面面俱到,绝对是名副其实的8分+!(ps:悄咪咪的说,其实这个工作量加上创新性冲击10分+也有可能哦)这个思路各个癌种均适用,不知道用啥思路能发高分的朋友,用这个多层面创新叠加思路做复现准没错,学起来吧!
选分析方向可以从最新发表文献入手,当然最便捷的方法当然还是持续关注小云公众号中的生信思路推荐,想定制创新性思路欢迎直接call小云。另外,还有我们的精品培训课程《肿瘤复发转移和耐药相关国自然热点方向思路设计专题会议》,有意向的小伙伴也欢迎咨询小云哦!


